题目内容
【题目】常温下0.1mol/L的H2A溶液中H2A、HA-、A2- 三者中所占物质的量分数随pH变化的关系如图所示.下列表述正确的是( )
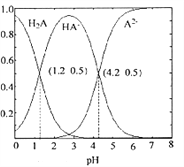
A. 在含H2A、HA-、A2-的溶液中,通入少量HCl,HA-的物质的量分数一定变大
B. 将等物质的量的NaHA、Na2A溶于水中,所得溶液中存在:c(Na+)+c(H+)=c(HA-)+c(A2-)+c(OH-)
C. 在 0.1mol/L NaHA 溶液中,各离子浓度大小关系为:
c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
D. 将等物质的量的NaHA、Na2A溶于水中,所得溶液pH恰好为4.2
【答案】C
【解析】A. 据图可知,随溶液pH增大,HA-的物质的量分数先增大后减小,在含H2A、HA-、A2-的溶液中,通入少量HCl,溶液pH减小,则HA-的物质的量分数可能增大也可能减小,故A错误;B. 将等物质的量的NaHA、Na2A溶于水中,根据电荷守恒可知:c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(OH-),故B错误;C. 据图可知,当HA-的物质的量分数最大时,溶液呈酸性,说明HA-的电离程度大于水解程度,在 0.1mol/L NaHA溶液中,因HA-发生电离,则c(Na+)>c(HA-),因水也能电离出H+,则c(H+)>c(A2-),溶液呈酸性,OH-的浓度最小,所以各离子浓度的大小关系为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-),故C正确;D. 将等物质的量的NaHA、Na2A溶于水中,若HA-和A2-浓度相等,则Ka2=![]() =10-4.2,c(H+)=10-4.2,pH=4.2,因HA-的电离程度大于水解程度,则溶液中c(A2-)>c(HA-),所得溶液pH不等于4.2,故D错误;答案选C。
=10-4.2,c(H+)=10-4.2,pH=4.2,因HA-的电离程度大于水解程度,则溶液中c(A2-)>c(HA-),所得溶液pH不等于4.2,故D错误;答案选C。

 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案


