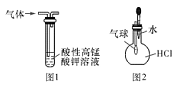��Ŀ����
��ѧ��ѧ�г����ļ������ʴ�����ͼ��ʾ��ת����ϵ�����У� A��һ�ֺ�ɫ��ĩ״���壬C��һ�ֻ���ɫ���壬ʵ�����г���E��Һ���ն����C����ͼ�в��ֲ���ͷ�Ӧ��������ȥ��
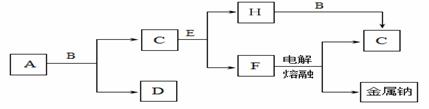
�ش��������⣺
��1��д��A��B��Ũ��Һ��Ӧ�Ļ�ѧ����ʽ ��
��2������E�к��л�ѧ���������� ��C��E��Ӧ�����ӷ���ʽΪ ��
��3����B��Ũ��Һ��H��Ũ��Һ��ϣ�����������������C���÷�Ӧ�����ӷ���ʽΪ
��
��4��ij����С���ͬѧ��E��Һ����C��������ͼ��ʾװ��������Һ�г���ͨ��SO2���塣
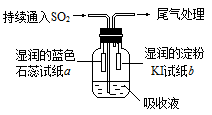
ʵ������й۲쵽��������
�ٿ�ʼʱ����Һ�Ϸ����ְ�������ֽa��졣��ͬѧ��Ϊ��HClʹa��죬��ͬѧ��ͬ��Ĺ۵㣬��ͬѧ����Ϊʹa������ ��д��һ�ּ��ɣ���
��Ƭ�̺���Һ�Ϸ����ֻ���ɫ���壬��ֽb�����������ӷ���ʽ����b������ԭ�� ��
��������ֽb��ɫ��ͬѧ����Ϊ���ܵ�ԭ�������֣�һ��I2�л�ԭ�ԣ�����ɫ��������ʽ���������IO3�����Ӷ�ʹ��ɫ��ʧ������ ��
��1�� MnO2 + 4HCl(Ũ) MnCl2 + Cl2��+ 2H2O��2�֣�
��2�� ���Ӽ������Լ���2�֣����һ�ָ�1�֣�
Cl2 +2OH��=== Cl��+ ClO��+ H2O��2�֣�
��3�� ClO��+ Cl��+ 2H+ === Cl2 �� + H2O��2�֣�
��4�� �� SO2����H2SO3�� ��2�֣�
�� Cl2 + 2I��=== 2Cl��+ I2��2�֣�
�� I2��������,SO2�ܽ�I2��ԭ��I�����Ӷ�ʹ��ɫ��ʧ��2�֣�

 ǧ�������������ĩ�����Ծ�����ϵ�д�
ǧ�������������ĩ�����Ծ�����ϵ�д�ij�¶��£�H2(g)��CO2(g)  H2O(g) ��CO(g)��ƽ�ⳣ��K��9/4�����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2(g)��CO2(g)������ʼŨ�������ʾ�������жϲ���ȷ����
H2O(g) ��CO(g)��ƽ�ⳣ��K��9/4�����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2(g)��CO2(g)������ʼŨ�������ʾ�������жϲ���ȷ����
| ��ʼŨ�� | �� | �� | �� |
| c(H2)/mol��L��1 | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol��L��1 | 0.010 | 0.010 | 0.020 |
A��ƽ��ʱ������CO2��ת���ʴ���60%
B��ƽ��ʱ�����кͱ���H2��ת���ʾ���60%
C��ƽ��ʱ������c(CO2)�Ǽ��е�2������0.012 mol��L��1
D����Ӧ��ʼʱ�����еķ�Ӧ������죬���еķ�Ӧ��������