题目内容
A、B、C、D、E五种元素,已知:
①A原子最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子M层上的电子比K层多5个.
②常温下B2是气体,它对氢气的相对密度是16.
③C的单质在B2中燃烧,生成淡黄色固体F.F与AB2反应可生成B2.
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2.D在DB2中的含量为50%.
根据以上情况回答:
(1)E位于第________周期,第________族;
(2)C的离子结构示意图是________,F中的化学键为________;
(3)AB2的结构式为________,其固体时所属的晶体类型是________;
(4)F和AB2反应的化学方程式________;
(5)常温下,E的单质与C的最高价氧化物对应水化物的水溶液反应的离子方程式为________.
答案:
解析:
解析:
|
本题综合考查了从物质结构、物质性质等方面对元素及物质化学式的推导.由元素原子核外电子排布规律可推知A为碳元素,E为氯元素.由相对密度知B2的相对分子质量为32,则B的相对原子质量为16,B为氧元素,AB2为CO2.由C的单质在B2中燃烧,生成淡黄色固体F,知C为钠,F为Na2O2.由D的单质在B2中燃烧,发出蓝紫色火焰,知D为S,DB2为SO2. |

练习册系列答案
相关题目



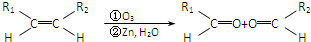

 元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )
元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )