题目内容
【题目】下列反应中水只表现还原性的是
A. 3NO2+H2O=2HNO3+NO
B. 2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
C. 2F2+2H2O=4HF+O2
D. 2Na+2H2O=2NaOH+H2↑
【答案】C
【解析】A项,N元素的化合价由NO2中的+4价部分升至HNO3中的+5价,部分降至NO中的+2价,H2O中H、O元素的化合价没有变化,H2O既不表现氧化性也不表现还原性;B项,H元素的化合价由H2O中+1价降为0价,O元素的化合价由H2O中-2价升至0价,H2O既表现氧化性又表现还原性;C项,F元素的化合价由0价降至HF中的-1价,F2表现氧化性,O元素的化合价由H2O中-2价升至0价,H2O只表现还原性;D项,Na元素的化合价由0价升至NaOH中的+1价,Na表现还原性,H元素的化合价由H2O中+1价降为H2中的0价,H2O只表现氧化性;答案选C。

【题目】以炼锌厂的烟道灰(主要成分为ZnO,另含少量Fe2O3、CuO、SiO2、MnO等)为原料可生产草酸锌晶体(ZnC2O42H2O). 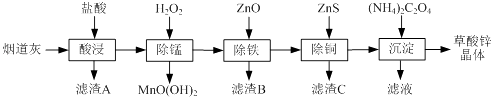
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 4.2 | 5.4 |
沉淀完全的pH | 3.3 | 9.7 | 6.7 | 8.2 |
请问答下列问题:
(1)滤渣A的主要成分为 .
(2)除锰过程中产生MnO(OH)2沉淀的离子方程式为 .
(3)①除铁(部分Cu2+可能被除去)时加入ZnO控制反应液pH的范围为 . ②上述流程中除铁与除铜的顺序不能颠倒,否则除铁率会减小,其原因是 .
(4)若沉淀过程采用Na2C2O4代替(NH4)2C2O4生产草酸锌晶体,合理的加料方式是 .
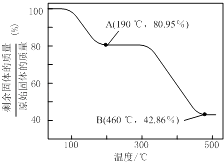
(5)将草酸锌晶体加热分解可得到一种纳米材料.加热过程中固体残留率随温度的变化如下图所示,300℃~460℃范围内,发生反应的化学方程式为