��Ŀ����
���û�ѧ��Ӧԭ���о�Ԫ�ؼ��仯����ķ�Ӧ����������������Ҫ���塣
��ش��������⣺
��1����ҵ���Ի�ͭ����Ҫ�ɷ� Cu2S��Ϊԭ�ϣ���ȡ��������������ͭ���ù����������·�Ӧ��
2Cu2S��s��+3O2��g��=2Cu2O��s��ʮ2SO2��g�� ��H=-768��2KJ��mol-1
2Cu2O��s��+Cu2S��s��=6Cu��s��+SO2��g�� ��H=+116��0KJ��mol-1
��ӦCu2S��s��+O2��g��=2Cu��s��+SO2��g���� ��H= ��
 ��2�������������漰��Ӧ��2SO
��2�������������漰��Ӧ��2SO![]() (g��+O
(g��+O![]() (g��
(g��![]() 2SO
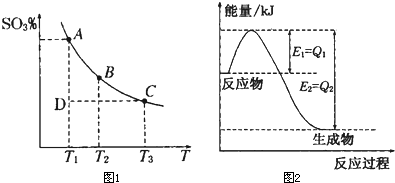
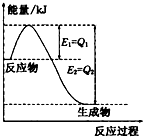
2SO![]() (g���� �� һ�������£���ƽ��ת���ʺ��¶ȵĹ�ϵ����ͼ��ʾ���÷�Ӧ�Ħ�H O�����������������Ӧ���е�״̬Dʱ��v�� v�������������������=������
(g���� �� һ�������£���ƽ��ת���ʺ��¶ȵĹ�ϵ����ͼ��ʾ���÷�Ӧ�Ħ�H O�����������������Ӧ���е�״̬Dʱ��v�� v�������������������=������
�� ij�¶�ʱ����4molSO2��2molO2ͨ��2L�ܱ������У�10minʱ��Ӧ�ﵽƽ��״̬�����SO3��Ũ��Ϊ1.6mol��L-1����0~10min�ڵ�ƽ����Ӧ����v��SO2��= �����¶��·�Ӧ��ƽ�ⳣ��K= ��
�� ����������֤���÷�Ӧ�Ѿ��ﵽ��ѧƽ��״̬���ǣ����ţ���ͬ��
A��������ѹǿ���ٷ����仯 B��SO![]() ������������ٷ����仯
������������ٷ����仯
C�������������������ٷ����仯 D�������������ܶȲ��ٷ����仯
�� ���²���������ƽ��������Ӧ�����ƶ��������SO![]() ת���ʵ���
ת���ʵ���
A����������ͨ������O![]() B����������ͨ������SO
B����������ͨ������SO![]()
C��ʹ�ô��� D�������¶� E������ͨ����������
�� ����SO2�Ǵ�����Ⱦ���ѡ�������Լ��е�_______���ա�
a��ŨH2SO4 b��ϡHNO3 c��NaOH��Һ d����
��1��-217.4KJ•mol-1��2�֣�
��2�� �٣�������ÿ��2�֣�
��0.16 mol��L��1��min��1��80 L��mol��1��ÿ��2�֣�
��A��B��2�֣�
��A����2�֣�
��c�� d��2�֣�

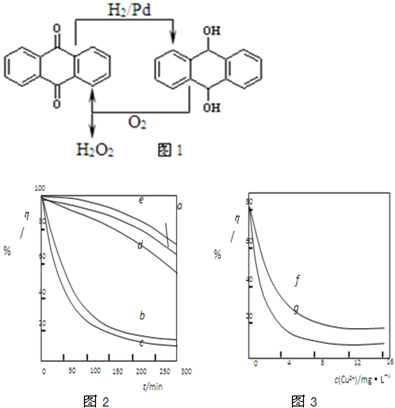
 ���û�ѧ��Ӧԭ���о������ȡ���ȵ��ʼ��仯����ķ�Ӧ����Ҫ���壮
���û�ѧ��Ӧԭ���о������ȡ���ȵ��ʼ��仯����ķ�Ӧ����Ҫ���壮