题目内容
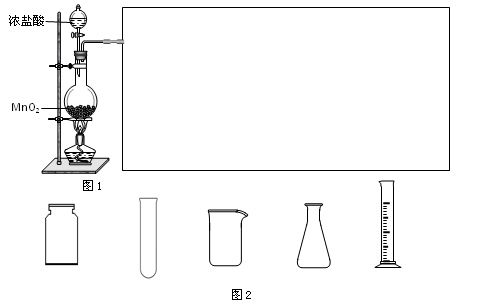
实验室用下面装置测定FeO和Fe2O3固体混合物中Fe2O3的质量,D装置的硬质双通玻璃管中的固体物质是FeO和Fe2O3的混合物。
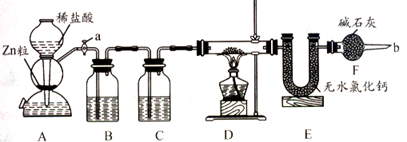
(1)如何检查装置A的气密性_________________________________________
(2)为了安全,在点燃D处的酒精灯之前,在b处必须_____________________。
(3) 装置B 的作用是_______________ ,装置C中装的液体是________________,所起的作用是_______________________。
(4)在气密性完好,并且进行了必要的安全操作后,点燃D处的酒精灯,在硬质双管中发生的化学反应方程式是________________________________________。
(5)若FeO和Fe2O3固体混合物的质量为31. 2g,反应完全后,U型管的质量增加9.9g则混合物中Fe2O3的质量为______________。
(6)U型管E右边连接干燥管F的目的是______________________,若无干燥管F,测得Fe2O3的质量将_____________(填“偏大”、“偏小”或“无影响”)

(1)如何检查装置A的气密性_________________________________________
(2)为了安全,在点燃D处的酒精灯之前,在b处必须_____________________。
(3) 装置B 的作用是_______________ ,装置C中装的液体是________________,所起的作用是_______________________。
(4)在气密性完好,并且进行了必要的安全操作后,点燃D处的酒精灯,在硬质双管中发生的化学反应方程式是________________________________________。
(5)若FeO和Fe2O3固体混合物的质量为31. 2g,反应完全后,U型管的质量增加9.9g则混合物中Fe2O3的质量为______________。
(6)U型管E右边连接干燥管F的目的是______________________,若无干燥管F,测得Fe2O3的质量将_____________(填“偏大”、“偏小”或“无影响”)
(1)关闭a ,往球形漏斗中加水,球形漏斗下端有一段水柱高于容器中液面,则装置气密(2)收集氢气验纯 (3)除HCl、 浓H2SO4 、 除水蒸气或干燥氢气
(4)Fe2O3 + 3H2 2Fe + 3H2O FeO + H2
2Fe + 3H2O FeO + H2  Fe + H2O(5)24g
Fe + H2O(5)24g
(6)防止空气中水蒸气进入、 偏大
(4)Fe2O3 + 3H2
 2Fe + 3H2O FeO + H2
2Fe + 3H2O FeO + H2  Fe + H2O(5)24g
Fe + H2O(5)24g (6)防止空气中水蒸气进入、 偏大
试题分析:本题实验原理是锌与稀盐酸产生氢气,氢气中混有氯化氢和水蒸气,B的作用是除去氯化氢、C的作用是除去水蒸气,D中发生两个反应(氢气还原氧化铁和氢气还原氧化亚铁),联想氢气还原氧化铜的实验,加热D中硬质玻璃管前,应先检验氢气的纯度。D中产生的水蒸气被无水氯化钙吸收,碱石灰的作用是吸收空气中的水蒸气,防止E增重质量偏大。设混合物中FeO和Fe2O3物质的量分别为x、y,由混合物总质量得72x+160y=31.2g;由U型管增重9.9g得x+3y=0.55mol,解得y=0.15mol、x=0.1mol,所以氧化铁质量为24g。若无干燥管F,则氧化铁质量偏大。
点评:分析误差时,设无干燥管时,U型管增重mg,则由72x+160y=31.2g、x+3y=m/18mol,解得y=(m-7.8)/14mol,所以若m偏大,则y偏大。

练习册系列答案
 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目