题目内容
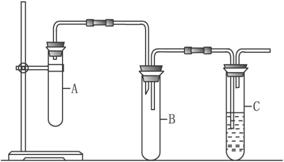
某化学课外活动小组为探究氮化合物的性质,设计了如图所示实验装置,A处是气体发生装置.
按如图连接好各仪器,检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的无色气体通过后面装置.片刻后可观察到F中Cu片慢慢溶解.请回答下列问题:
(1)A中制取气体时只使用一种药品,它可以是
a.NH4HCO3固体 b.NH4C1固体 C.NaHCO3固体d.浓氨水
在以上几种情况下A装置中均适用的玻璃仪器有
a.烧瓶 b.试管 c.烧杯d.锥形瓶 e.酒精灯
(2)E装置可防止F中溶液倒吸进入D,请在图中画出装置E中的导气管.
(3)写出C中发生反应的化学方程式
(4)若进入F装置的物质成分和质量一定,可向F中加入下列物质中的
a.Na2 CO3 b.NaCl c.CuSO4 d.H2SO4
(5)指导老师认为他们设计的这套实验装置还存在一处明显的缺陷,改进建议为
分析:(1)根据题中信息推断装置A中产生的气体,然后根据要求判断药品;根据反应原理选择使用的仪器;
(2)根据E的作用是防止F中溶液倒吸进入D分析导气管长短情况;
(3)C中发生反应为氨气和氧气在催化剂作用下发生氧化还原反应生成一氧化氮和水;根据该反应为放热反应分析C处加热片刻后撤去酒精灯,铂丝仍保持红热原因;
(4)根据铜与稀硝酸反应的离子方程式判断氢离子和硝酸根离子消耗情况;
(5)没有处理尾气,尾气中的有毒气体会污染空气,应加上尾气处理装置.
(2)根据E的作用是防止F中溶液倒吸进入D分析导气管长短情况;
(3)C中发生反应为氨气和氧气在催化剂作用下发生氧化还原反应生成一氧化氮和水;根据该反应为放热反应分析C处加热片刻后撤去酒精灯,铂丝仍保持红热原因;
(4)根据铜与稀硝酸反应的离子方程式判断氢离子和硝酸根离子消耗情况;
(5)没有处理尾气,尾气中的有毒气体会污染空气,应加上尾气处理装置.
解答:解:(1)根据题意:C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯,铂丝继续保持红热,F处铜片逐渐溶解,说明有硝酸生成,所以A中获得的是氨气,加热NH4HCO3或浓氨水都可以产生氨气,制取氨气反应中A装置均适用的玻璃仪器有试管和酒精灯,
故答案为:ad;be;
(2)由于E的作用是防止F中溶液倒吸进入D,所以连接D的导管不能够伸入集气瓶底部即可,如图: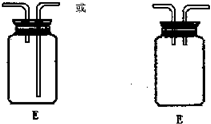 ,
,
故答案为: ;
;
(3)C中氨气与氧气发生了氧化还原反应,反应的方程式为:4NH3+5O2
4NO+6H2O,由于该反应为放热反应,C处加热片刻后撤去酒精灯,铂丝仍保持红热,
故答案为:4NH3+5O2
4NO+6H2O;该反应为放热反应;
(4)根据反应可知,3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,反应中消耗的氢离子物质的量大于硝酸根离子的物质的量,所以向溶液中只要加入氢离子,就可以溶解更多的铜,所以应该加入硫酸,故选d;
(5)铜和硝酸反应的产物一氧化氮以及生成的二氧化氮均有毒,能够污染大气,应加一个尾气吸收装置,故答案为:应在F后面加上尾气处理装置.
故答案为:ad;be;
(2)由于E的作用是防止F中溶液倒吸进入D,所以连接D的导管不能够伸入集气瓶底部即可,如图:
 ,
,故答案为:
 ;
;(3)C中氨气与氧气发生了氧化还原反应,反应的方程式为:4NH3+5O2
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
(4)根据反应可知,3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,反应中消耗的氢离子物质的量大于硝酸根离子的物质的量,所以向溶液中只要加入氢离子,就可以溶解更多的铜,所以应该加入硫酸,故选d;
(5)铜和硝酸反应的产物一氧化氮以及生成的二氧化氮均有毒,能够污染大气,应加一个尾气吸收装置,故答案为:应在F后面加上尾气处理装置.
点评:本题主要考查学生氨气的化学性质,题目难度较大,结合实验的方式来考查,增大了难度,要求学生熟练掌握氨气的制法及化学性质,是高考中的常见题型,对学生的思维能力提出了较高的要求,充分考查了学生灵活应用所学知识解决实际问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某化学课外活动小组为探究铜与硝酸反应还原产物主要为NO时硝酸的浓度,设计实验装置如下图所示(连接好仪器并检查气密性后,分别装入相对应的试剂):

Ⅰ.(1)实验开始时先打开活塞K持续通入N2一段时间后,并闭K。将铜丝(足量)下移伸入浓硝酸后,有大量的红棕色气体生成,随时间的进行,气体颜色逐渐变浅,当A中充满无色气体时:
①装置A中反应的离子方程式为___________________________。
②接下来的实验操作是___________________________________。
(2)本实验中装置A的优点是____________________________。
Ⅱ.将B中所得溶液稀释至200 mL,用0.20 mol/L的NaOH溶液进行滴定。实验数据如下(硝酸的挥发分解及溶液体积的变化忽略不计):
实验编号 | 待测液体积(mL) | NaOH溶液体积(mL) |
1 | 20.00 | 15.98 |
2 | 20.00 | 14.99 |
3 | 20.00 | 15.01 |
(1)待测液的浓度为____________mol/L。
(2)硝酸与铜反应主要生成NO时硝酸的浓度不大于____________mol/L。