题目内容
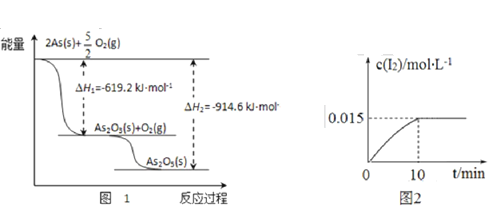
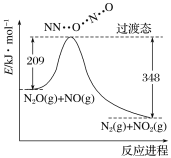
【题目】由N2O和NO反应生成N2和NO2的能量变化如图所示。下列说法不正确的是( )
A.反应生成1 mol N2时转移4 mol e-
B.反应物能量之和大于生成物能量之和
C.N2O(g)+NO(g)=N2(g)+NO2(g) ΔH=-139 kJ·mol-1
D.断键吸收能量之和小于成键释放能量之和
【答案】A
【解析】
A. 化学方程式:N2O+NO = N2+NO2,生成1 mol N2时转移电子2 mol,故A错误;
B. 根据能量变化图,反应物的总能量大于生成物的总能量,此反应属于放热反应,故B正确;
C. 根据能量变化图,N2O(g) +NO(g) = N2(g) +NO2(g) ΔH=(209-348) kJ·mol1=-139 kJ·mol1,故C正确;
D. 断键吸收能量,成键释放能量,此反应是放热反应,因此断键吸收能量之和小于成键释放能量之和,故D正确。
综上所述,答案为A。

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
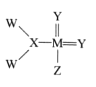
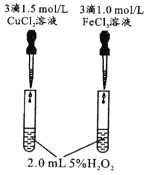
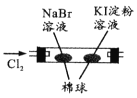
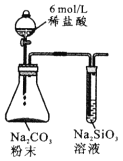
【题目】由下列实验现象一定能得出相应结论的是
选项 | A | B | C | D |
装置图 |
|
|
|
|
现象 | 右边试管产生气泡较快 | 左边棉球变棕黄色,右边棉球变蓝色 | 试管中先出现淡黄色固体,后出现黄色固体 | 试管中液体变浑浊 |
结论 | 催化活性:Fe3+>Cu2+ | 氧化性:Br2>I2 | Ksp:AgCl>AgBr>AgI | 非金属性:C>Si |
A. AB. BC. CD. D