题目内容
【题目】铅和铅的化合物有广泛的用途,如Pb有感光性,也可用作金属着色剂,PbI2在潮湿空气中能被光逐渐分解,生成一氧化铅和碘。合成PbI2的实验流程如图所示。
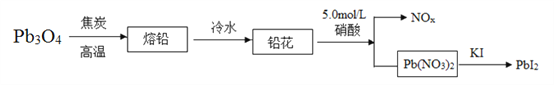
(1)若Fe3O4表示为氧化物形式是Fe2O3·FeO,将Pb3O4表示为氧化物形式是__________。
(2)将铅块制成铅花的目的是_______________。
(3)如果流程中生成的NOx为NO,则氧化剂与还原剂的物质的量之比为__________。
(4)PbI2在潮湿空气中能被光逐渐分解的化学方程式为_______________。
(5)硫酸铅可溶于醋酸铵饱和溶液中,请从化学反应原理角度解释:_____________________。
(6)铅主要的矿物有方铅矿(PbS)和铅钒矿(PbSO4),将二者以物质的量之比为1:1时加热得到金属铅和一种气体,有关反应的化学方程式是__________________。
(7)室温下,浓度均为4×10-3mo/L的KI和Pb(NO3)2溶液等体积混合,刚好能生成PbI2沉淀,则室温时PbI2的Ksp为___________。
【答案】 PbO2·2PbO 是为了增大与酸反应的接触面积,加快溶解反应速率 2:3 2PbI2+O2=2PbO+2I2 两者可反应生成难电离的可溶性盐(CH3COO)2Pb PbS+PbSO4![]() 2Pb+2SO2↑ 8.0×10-9
2Pb+2SO2↑ 8.0×10-9
【解析】(1)若Fe3O4表示为氧化物形式是Fe2O3·FeO,根据铅的主要化合价为+2和+4,可以将Pb3O4用氧化物形式表示为PbO2·2PbO。
(2)将铅块制成铅花的目的是为了增大与酸反应的接触面积,加快溶解反应速率。
(3)如果流程中生成的NOx为NO,则该反应的化学方程式为3Pb+8HNO3=3Pb(NO3)2+2NO↑+4H2O,其中氧化剂与还原剂的物质的量之比为2:3。
(4)由题意知,PbI2在潮湿空气中能被光逐渐分解,生成一氧化铅和碘,该反应的化学方程式为2PbI2+O2=2PbO+2I2。
(5)硫酸铅可溶于醋酸铵饱和溶液中,说明两者可发生复分解反应,生成难电离的可溶性盐(CH3COO)2Pb。
(6)铅主要的矿物有方铅矿(PbS)和铅钒矿(PbSO4),将二者以物质的量之比为1:1时加热得到金属铅和一种气体。根据质量守恒定律可知,该反应的化学方程式是PbS+PbSO4![]() 2Pb+2SO2↑。
2Pb+2SO2↑。
(7)室温下,浓度均为4×10-3mo/L的KI和Pb(NO3)2溶液等体积混合后,溶液中碘离子浓度和铅离子浓度均为2×10-3mo/L,因为刚好能生成PbI2沉淀,则室温时PbI2的Ksp为(2×10-3)3=8.0×10-9。

 阅读快车系列答案
阅读快车系列答案



