题目内容
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D 同族,C的简单离子和B的简单离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物中阴阳离子的个数比为1:1。回答下列问题:
(1)五种元素中,原子半径最大的是____________(填元素名称),非金属性最强元素的是___________。
(2)由元素A分别和元素B、D、E所形成的共价型化合物中,热稳定性最差的是
______________(用化学式表示)。
(3)元素A和E形成的化合物与元素A和B形成的化合物反应,产物的电子式为_________________,其中存在的化学键类型为_________________________。
(4)E离子的结构示意图是____________________;
元素D最高价氧化物的水化物的化学式为_________________。
(5)单质E与水反应的离子方程式为 ____________________________________。
【答案】 钠 氯 PH3 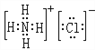 离子键和共价键
离子键和共价键 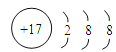 H3PO4或HPO3 Cl2+ H2O== H++ Cl-+ HClO
H3PO4或HPO3 Cl2+ H2O== H++ Cl-+ HClO
【解析】五种短周期元素A﹑B﹑C﹑D﹑E的原子序数依次增大,A和B形成的化合物在水中呈碱性,则化合物为氨气,则A为H,B为N;A和C同族,B和D同族,C离子和B离子具有相同的电子层结构,则C为Na、D为P;A和B﹑D﹑E均能形成共价型化合物,C和E形成CE型的化合物,则E的化合价为-1,最外层含有7个电子,原子序数大于Na,则E为Cl元素。
(1)电子层越多、原子半径越大,电子层相同时,核电荷数越小,原子半径越大,则上述元素中,Na原子半价最大;同一周期中,原子序数越大,非金属性越强,则Cl的非金属性最强,故答案为:Na;Cl;
(2)非金属性Cl>P,N>P,则热稳定性最差的是为PH3,故答案为:PH3;
(3)HCl与氨气反应生成氯化铵,化学式为NH4Cl,氯化铵属于离子化合物,电子式为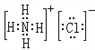 ,其中存在离子键、共价键,故答案为:
,其中存在离子键、共价键,故答案为: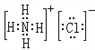 ;离子键和共价键;
;离子键和共价键;
(4)P元素的最高价氧化物的水化物的化学式为H3PO4或HPO3,故答案为:H3PO4或HPO3;
(5)E的单质为氯气,氯气与水反应生成盐酸与次氯酸,反应离子方程式为:Cl2+H2O=H++Cl-+HClO,故答案为:Cl2+H2O=H++Cl-+HClO。

 名校课堂系列答案
名校课堂系列答案