题目内容
1.92 g Cu投入到一定量的浓HNO3中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672 mL气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入O2的体积为( )
A. 336 mL B.504 mL C.224 mL D.168 mL
【答案】
A
【解析】
试题分析:Cu和浓硝酸反应产生的气体通入氧气后能够被水全部吸收又转变成了硝酸,所以Cu失的电子全部被氧气得到,1.92gCu失电子数为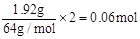 ,1mol氧气得4mol 电子,所以氧气的物质的量为
,1mol氧气得4mol 电子,所以氧气的物质的量为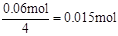 ,体积为0.015mol×22.4L/mol=336 mL。答案选A。
,体积为0.015mol×22.4L/mol=336 mL。答案选A。
考点:金属与硝酸反应的计算
点评:本题用守恒法最简单,这类习题也是高考的重点习题,主要考查学生的分析能力,难度较大。

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
1.92 g Cu投入到一定量的浓HNO3中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672 mL气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入O2的体积为( )
| A.336 mL | B.504 mL | C.224 mL | D.168 mL |