题目内容
1.92 g Cu投入到一定量的浓硝酸中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672 ml气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入O2的体积为
A.504 ml B.336 ml????? C.224 ml? ?????? D.168 ml
【答案】
B
【解析】
试题分析:1.92g Cu的物质的量为n(Cu)=1.92g÷64g/mol=0.03mol,反应时失去电子数目为2×0.03mol=0.06mol,反应整个过程为HNO3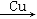 NO、NO2
NO、NO2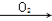 HNO3,反应前后HNO3的物质的量不变,而化合价变化的只有铜和氧气,则Cu失去电子数目等于O2得到电子的数目,所以消耗氧气的物质的量为n(O2)=0.06mol÷4=0.015mol,V(O2)=0.015mol×22400ml/mol=336ml,所以通入O2的体积为336ml,故答案选B。
HNO3,反应前后HNO3的物质的量不变,而化合价变化的只有铜和氧气,则Cu失去电子数目等于O2得到电子的数目,所以消耗氧气的物质的量为n(O2)=0.06mol÷4=0.015mol,V(O2)=0.015mol×22400ml/mol=336ml,所以通入O2的体积为336ml,故答案选B。
考点:考查氧化还原反应的有关计算

练习册系列答案
相关题目
1.92 g Cu投入到一定量的浓HNO3中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672 mL气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入O2的体积为( )
| A.336 mL | B.504 mL | C.224 mL | D.168 mL |