题目内容
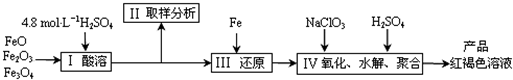
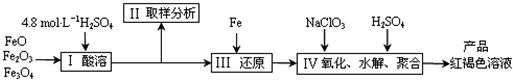
Ⅰ将一定质量的铁粉加入到装有100mL某浓度的稀硝酸溶液中充分反应。
(1)容器中剩有mg的铁粉,收集到NO气体448mL(标准状况下)。
① 所得溶液中的溶质的化学式是_______________;
② 原硝酸溶液的物质的量浓度为:________________mol/L
(2)向上述固-液混合物中逐滴加入稀硫酸直到刚好不再产生气体为止,该气体遇空气变成红棕色。此时容器中有铁粉ng。
①此时溶液中溶质的化学式是__________;
②m-n的值为_____________g 。
Ⅱ:向某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间的变化如下图中甲图所示。附图中乙图为t2时刻后改变容器中条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件,所用条件均不同。已知t3~t4阶段为使用催化剂[已知
t0~ t1阶段c ( B)未画出]。
(3)若 t1=15s ,则t0~ t1阶段以C浓度变化表示的反应速率为________________;
(1)容器中剩有mg的铁粉,收集到NO气体448mL(标准状况下)。
① 所得溶液中的溶质的化学式是_______________;
② 原硝酸溶液的物质的量浓度为:________________mol/L
(2)向上述固-液混合物中逐滴加入稀硫酸直到刚好不再产生气体为止,该气体遇空气变成红棕色。此时容器中有铁粉ng。
①此时溶液中溶质的化学式是__________;
②m-n的值为_____________g 。
Ⅱ:向某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间的变化如下图中甲图所示。附图中乙图为t2时刻后改变容器中条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件,所用条件均不同。已知t3~t4阶段为使用催化剂[已知
t0~ t1阶段c ( B)未画出]。
(3)若 t1=15s ,则t0~ t1阶段以C浓度变化表示的反应速率为________________;
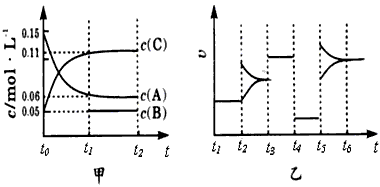
(4)t4~t5阶段改变的条件为____________,B的起始物质的量为______________;
(5)t5~t6阶段容器内A的物质的量共减少0. 03mol ,而此过程中容器与外界的热交换总量为akJ,写出该反应的热化学方程式________________________。
(5)t5~t6阶段容器内A的物质的量共减少0. 03mol ,而此过程中容器与外界的热交换总量为akJ,写出该反应的热化学方程式________________________。
(1)①Fe(NO3)2
② 0.8
(2)①FeSO4 ②5.04
(3)0.004mol·L-1·s-1
(4)减小压强;0.04mol
(5)3A(g)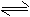 2C(g)+B(g);ΔH=+100akJ·mol-1
2C(g)+B(g);ΔH=+100akJ·mol-1
② 0.8
(2)①FeSO4 ②5.04
(3)0.004mol·L-1·s-1
(4)减小压强;0.04mol
(5)3A(g)
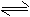 2C(g)+B(g);ΔH=+100akJ·mol-1
2C(g)+B(g);ΔH=+100akJ·mol-1
练习册系列答案
相关题目