题目内容
(8分)某待测液中可能含有Ag+、Fe3+、K+、Ba2+、NH4+等离子,进行如下实验:
(1)加入过量的稀盐酸,有白色沉淀生成。
(2)过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
(3)过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现。
(4)另取少量步骤(3)中的滤液,加入NaOH溶液至使溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:待测液中一定含有 离子;
一定不含有 离子;还有_________________离子不能确定是否存在,要检验这些离子的实验方法是 ,操作是______________________________________________。
(1)加入过量的稀盐酸,有白色沉淀生成。
(2)过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
(3)过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现。
(4)另取少量步骤(3)中的滤液,加入NaOH溶液至使溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:待测液中一定含有 离子;
一定不含有 离子;还有_________________离子不能确定是否存在,要检验这些离子的实验方法是 ,操作是______________________________________________。
Ag+、Ba2+、NH4+ ;Fe3+;K+ ;焰色反应;用铂丝沾取溶液在酒精灯上灼烧并透过蓝色钴玻璃观察火焰颜色
加入过量的稀盐酸,有白色沉淀生成,说明含有银离子。根据(2)可知溶液中含有钡离子。根据(3)可知溶液中没有铁离子。根据(4)可知气体是氨气,说明含有NH4+。所以待测液中一定含有Ag+、Ba2+、NH4+;一定不含有Fe3+;可能含有K+。钾离子的检验,可以用焰色反应,即用铂丝沾取溶液在酒精灯上灼烧并透过蓝色钴玻璃观察火焰颜色。

练习册系列答案
相关题目

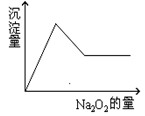
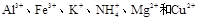 等离子中的一种或几种。现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀。如加入Na2O2的量与生成白色沉淀的量之间的关系用下图来表示。
等离子中的一种或几种。现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀。如加入Na2O2的量与生成白色沉淀的量之间的关系用下图来表示。