题目内容
称取两份铝粉,第一份加入足量的浓氢氧化钠溶液,第二份加入足量的稀盐酸,如要放出等体积的气体(在同温同压下),两份铝的质量之比为……( )
| A.1:2 | B.1:3 | C.3:2 | D.1:1 |
D
铝能与酸及强碱溶液发生氧化还原反应放出氢气。反应中铝均作还原剂,而产生的氢气都是由H+(盐酸或水中)得电子被还原而成的,根据在氧化还原反应中得、失电子总数相等的原则,可快速求解。
铝与盐酸反应时,由Al→Al3+;铝与浓NaOH反应时,Al→AlO2-,每摩铝均失去3摩电子。而产生氢气都是由H+(盐酸或水中)得电子被还原:2H++2e=H2↑,根据氧化还原反应中得失电子总数相等的原则,既然放出氢气的体积相等,那么在两个反应中消耗的铝的物质的量一定相等,故质量也相等,即应选D。
铝与盐酸反应时,由Al→Al3+;铝与浓NaOH反应时,Al→AlO2-,每摩铝均失去3摩电子。而产生氢气都是由H+(盐酸或水中)得电子被还原:2H++2e=H2↑,根据氧化还原反应中得失电子总数相等的原则,既然放出氢气的体积相等,那么在两个反应中消耗的铝的物质的量一定相等,故质量也相等,即应选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
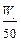 mol
mol 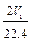 mol
mol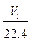
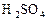 反应,生成
反应,生成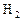 2.8L(标准状况),原混合物的质量可能是( )
2.8L(标准状况),原混合物的质量可能是( )
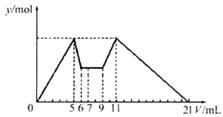
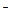 )=1:1:14
)=1:1:14