题目内容
将质量为W1 g的钠、铝混合物投入一定量的水中充分反应,金属没有剩余,溶液澄清,共收集到标准状况下的气体V1 L。向溶液中逐滴加入浓度为a mol/L的盐酸,过程中有白色沉淀生成后又逐渐溶解,当沉淀恰好消失时所加盐酸体积为V2 L,将溶液在HCl气氛中小心蒸干得固体W2 g。下列所列关系式中正确的是 ( )
| A.35.5a=(W2-W1) V2 |
B.n(Al)>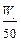 mol mol |
C.n(Na)+3n(Al)=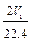 mol mol |
D. aV2=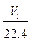 |
C
命题意图:考察高中化学钠和铝有关化学性质。
思路点拨:本题是一道综合了钠和铝有关化学性质的较难的计算型选择题,题目融合了化学中的“初态——终态”思想以及在化学选择和计算题中普遍使用的守恒法。根据题意,W1 g的Na和Al经过和一定量的水反应,置换出了V1 L H2,由电子得失守恒知:Na和Al完全反应变成Na+和Al3+失去的电子数应该等于生成的H2得到的电子数,则有n(Na)+3n(Al)=2V1/22.4 ;且Al要完全溶解 ,必须使生成的n(NaOH)>n(Al),假设n(Al)=n(NaOH)=n(Na),则有23n(Na)+27n(Al)=W1,得n(Al)<W1/50 ;溶液经过一系列的反应最终得到的固体应该是NaCl和AlCl3的混合固体,因此,由“初态(Na和Al)——终态(NaCl和AlCl3)”知W2-W1是盐酸中Cl元素的质量,则有35.5aV2=W2-W1 ;aV2可看成是盐酸中Cl元素的物质的量,由Cl元素守恒知aV2=n(Na)+3n(Al)=2V1/22.4。
思路点拨:本题是一道综合了钠和铝有关化学性质的较难的计算型选择题,题目融合了化学中的“初态——终态”思想以及在化学选择和计算题中普遍使用的守恒法。根据题意,W1 g的Na和Al经过和一定量的水反应,置换出了V1 L H2,由电子得失守恒知:Na和Al完全反应变成Na+和Al3+失去的电子数应该等于生成的H2得到的电子数,则有n(Na)+3n(Al)=2V1/22.4 ;且Al要完全溶解 ,必须使生成的n(NaOH)>n(Al),假设n(Al)=n(NaOH)=n(Na),则有23n(Na)+27n(Al)=W1,得n(Al)<W1/50 ;溶液经过一系列的反应最终得到的固体应该是NaCl和AlCl3的混合固体,因此,由“初态(Na和Al)——终态(NaCl和AlCl3)”知W2-W1是盐酸中Cl元素的质量,则有35.5aV2=W2-W1 ;aV2可看成是盐酸中Cl元素的物质的量,由Cl元素守恒知aV2=n(Na)+3n(Al)=2V1/22.4。

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目