题目内容
2.元素周期表中第 VIIA族元素的单质及其化合物的用途广泛.(1)与氯元素同族的短周期元素的原子结构示意图为
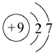 .
.(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据为B、C(填字母).
A.Cl2、Br2、I2的熔点 B. Cl2、Br2、I2的氧化性
C.HCl、HBr、HI的热稳定性 D. HCl、HBr、HI的酸性
(3)一定条件,在水溶液中1mol Cl-、ClOx-(x=1,2,3,4)的能量(KJ)相对大小如图所示.
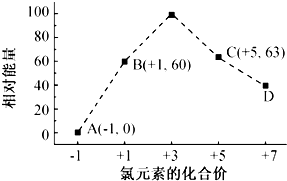
①D为ClO4-(填离子符号).
②B→A+C反应的热化学方程式为3ClO-(aq)=ClO3-(aq)+2Cl-(aq)△H=-117kJ/mol(用离子符号表示).
(4)某化合物是一种不稳定的物质,其分子组成可用OxFy表示,10mLOxFy气体能分解生成15mLO2和10mLF2(同温同压).
①该化合物的化学式为O3F2.
②已知该化合物分子中x个氧原子呈…O-O-O…链状排列,则其电子式为
 ,…O-O-O…链状排列中中间氧的价态为0.
,…O-O-O…链状排列中中间氧的价态为0.
分析 (1)与氯元素同族的短周期元素为F;
(2)同一主族元素,元素的非金属性随着原子序数增大而减弱,元素的非金属性越强,其气态氢化物越稳定、其单质的氧化性越强、其最高价氧化物的水化物酸性越强、与氢气化合越容易;
(3)一定条件下,在水溶液1 mol Cl-、ClOx-(x=1,2,3,4,)的能量(kJ)相对大小如图所示.
①D中Cl元素化合价为+7价,据此判断x值;
②B→A+C,根据转移电子守恒得该反应方程式为3ClO-=ClO3-+2Cl-,反应热=(63kJ/mol+2×0kJ/mol)-3×60kJ/mol=-117kJ/mol;
(4)①根据方程式中各物质的物质的量之比等于计量数之比,相同条件下的各气体的物质的量之比等于其体积之比,计确定A的分子式.
②根据分子式结合已知条件写其分子式,根据F显-1价分析.
解答 解:(1)与Cl同一主族是短周期元素是F元素,F原子核外有2个电子层、最外层7个电子,其原子结构示意图为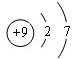 ,故答案为:
,故答案为: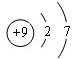 ;
;
(2)同一主族元素,元素的非金属性随着原子序数增大而减弱,元素的非金属性越强,其气态氢化物越稳定、其单质的氧化性越强、其最高价氧化物的水化物酸性越强、与氢气化合越容易,
故答案为:BC;
(3)①根据图象知,D中Cl元素化合价为+7价,所以ClOx-中x为4,则D为ClO4-,故答案为:ClO4-;
②B→A+C,根据转移电子守恒得该反应方程式为3ClO-=ClO3-+2Cl-,反应热=(63kJ/mol+2×0kJ/mol)-3×60kJ/mol=-117kJ/mol,所以该热化学反应方程式为3ClO-(aq)=ClO3-(aq)+2Cl-(aq)△H=-117kJ/mol,
故答案为:3ClO-(aq)=ClO3-(aq)+2Cl-(aq)△H=-117kJ/mol;
(4)根据原子守恒配平方程式,
OxFy =$\frac{x}{2}$O2 +$\frac{y}{2}$F2,
1×22.4L $\frac{x}{2}$×22.4L $\frac{y}{2}$×22.4L
10mL 15mL 10mL
所以x=3;y=2;
故答案为:O3F2
(2)该分子中含3个O原子,根据“A分子中X个氧原子是…-O-O-O-…链状排列”知,两个F原子位于该分子的两端,所以该分子的结构式为F-O-O-O-F,电子式为 ,F显-价,则两端的O原子显+1价,所以中间的O原子显0价.
,F显-价,则两端的O原子显+1价,所以中间的O原子显0价.
故答案为: ,0.
,0.
点评 本题考查较综合,涉及原子结构、物质性质、元素周期律、盖斯定律的应用、电子式等知识点,同时考查学生分析问题、解答问题能力,知道金属性、非金属性强弱判断方法,题目难度中等.

| A. | 0.1b/a mol•L-1 | B. | 1×10-1 mol•L-1 | ||
| C. | 1×10-7 mol•L-1 | D. | 0.1b/(a+b) mol•L-1 |
| A. | 2,2-二甲基丙烷和2-甲基丁烷互为同分异构体 | |
| B. | 沸点:正戊烷>正丁烷>2-甲基丙烷 | |
| C. | 分子式分别为C5H12、C9H20和C100H202的有机物一定互为同系物 | |
| D. | 含有5个碳原子的烃有三种同分异构体 |
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(2)镁的原子结构示意图为
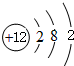 .
.(3)N与O原子半径较大的是N.
(4)H2SO4与HClO4中,酸性较强的是HClO4.
(5)NaOH与Al(OH)3中,属于两性氢氧化物的是,它常用作治疗胃酸(含盐酸)过多的药物,该反应的离子方程式为Al(OH)3+3H+=Al3++3H2O.
(6)Si是良好的半导体材料,它的氧化物常用于制造光导纤维(填一种高性能的现代通讯材料).
(7)碳元素形成的一种氧化物的化学式是?CO或CO2,该物质中C元素与O元素的质量比为3:4或3:8?.(相对原子质量:C-12 O-16)
| A. | +92.3 kJ•mol-1 | B. | -92.3 kJ•mol-1 | C. | -184.6 kJ•mol-1 | D. | +184.6 kJ•mol-1 |
| A. | H2O2 | B. | Na2O2 | C. | H2S | D. | Mg(NO3)2 |
 .有关柠檬烯的分析正确的是( )
.有关柠檬烯的分析正确的是( )| A. | 它的一氯代物有6种 | |
| B. | 它和丁基苯( )互为同分异构体 )互为同分异构体 | |
| C. | 一定条件下,它分别可以发生加成、取代、氧化反应 | |
| D. | 它的分子中所有的碳原子一定在同一个平面上 |
 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、醋酸,D中放有饱和碳酸钠溶液.请回答:
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、醋酸,D中放有饱和碳酸钠溶液.请回答: CH3CO18OC2H5+H2O.
CH3CO18OC2H5+H2O.