题目内容
将2.000g Na2SO4、Na2CO3和NaNO3的混合物溶于水得溶液A,在A中加入足量未知浓度的BaCl2溶液10.00mL,然后过滤得沉淀B 3.315g和滤液C;在C中加入足量的AgNO3溶液,又生成5.740g沉淀;向B中加入足量稀硫酸,充分反应后,沉淀质量变为3.495g.计算:
(1)氯化钡溶液的物质的量浓度.
(2)原混合物中硝酸钠的质量分数.
答案:
解析:
解析:
|
(1)n(Cl-)= c(BaCl2)= (2)Na2CO3~BaCO3~BaSO4 Δm 1mol 197g 233g 36g n(Na2CO3)=(3.495g-3.315g)÷36g·mol-1=0.005mol n(Na2SO4)=(3.315g-0.005mol×197g·mol-1)÷233g·mol-1=0.01mol m(NaNO3)=2.000g-0.005mol×106g·mol-1-0.01mol×142g·mol-1=0.05g w(NaNO3)=0.050g÷2.000g=0.025(2.5%) |

练习册系列答案
相关题目
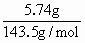 =0.04mol
=0.04mol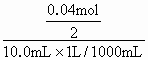 =2.01mol/L
=2.01mol/L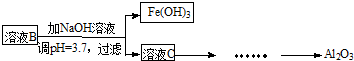 硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3(约10%)和MgO(约5%).某同学设计了如下方案,分离样品中各种金属元素.请回答下列问题.
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3(约10%)和MgO(约5%).某同学设计了如下方案,分离样品中各种金属元素.请回答下列问题.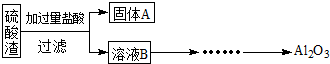
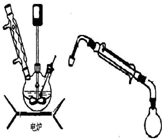 水合肼作为一种重要的精细化工原料,在农药、医药及有机合成中有广泛用途. 用尿素法制备水合肼,可分为两个阶段,第一阶段为低温氯化阶段,第二阶段为高温水解阶段,总反应方程式为:(NH2)2CO+NaClO+2NaOH→H2N-NH2?H2O+NaCl+Na2CO3.
水合肼作为一种重要的精细化工原料,在农药、医药及有机合成中有广泛用途. 用尿素法制备水合肼,可分为两个阶段,第一阶段为低温氯化阶段,第二阶段为高温水解阶段,总反应方程式为:(NH2)2CO+NaClO+2NaOH→H2N-NH2?H2O+NaCl+Na2CO3.