题目内容
下图是氢氧化钠试剂标签上的部分数据。两位同学欲测定该试剂是否为合格产品。

(1)甲同学的做法是:
①将2.000g该试剂溶于水配成250mL溶液,所需的主要仪器除玻璃棒、量筒、胶头滴管外,还须玻璃仪器有 、 。
②取上述溶液25.00mL放入锥形瓶中,加2滴甲基橙作指示剂,用0.2000mol?L―1的标准盐酸滴定至终点(其它杂质不与盐酸反应)。假定其它步骤都合理正确。请你分析根据消耗盐酸的体积 (填“能”或“不能”)测出NaOH的含量。
(2)乙同学设计的实验方案是:将2.000g该试剂溶于适量的水,加入足量的BaCl2溶液,充分反应后,过滤、洗涤、烘干,称量沉淀的质量,就可以计算出Na2CO3的含量。乙同学设计的实验方案是否合理? (填“合理”或“不合理”)。若不合理,请说明理由 。
(1)①250mL 容量瓶 烧杯 ②不能
(2)不合理 试剂中含有可溶性杂质、硫酸盐也可与BaCl2溶液反应生成沉淀

练习册系列答案
相关题目
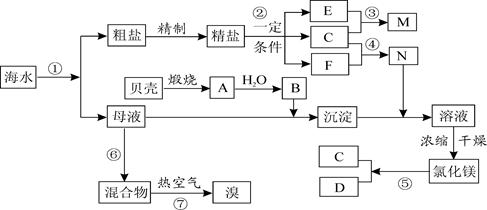
 单质处循环
单质处循环 (填“甲”或“乙”),理由是 。
(填“甲”或“乙”),理由是 。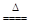 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O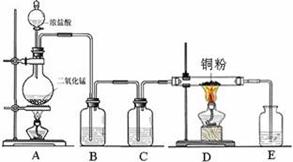
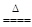 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O 
 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。