题目内容
【题目】在盛有足量A的体积可变的密闭容器中,加入B,发生反应:A(s)+2B(g)![]() 4C(g)+D(g);△H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是
4C(g)+D(g);△H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是
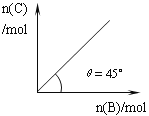
A. 若保持压强一定,当温度升高后,则图中θ>45°
B. 若再加入B,则再次达到平衡时正、逆反应速率均逐渐增大
C. 若保持压强一定,再加入B,则反应体系气体密度减小
D. 平衡时B的转化率为50%
【答案】D
【解析】试题分析:A、温度升高,平衡逆向移动,一定物质的量的B反应生成的C的物质的量减少,所以角度变小,错误,不选A;B、加入B,平衡正向移动,正反应速率突然增大,逆反应速率不变,平衡开始移动,正反应速率减慢,逆反应速率增大,错误,不选B;C、根据图像分析,加入的B的物质的量与生成C的物质的量相等,所以该反应中有一半的B物质反应,假设加入的B的物质的量为nmol,则
A(s)+2B(g) 4C(g)+D(g)
起始 n/2 n 0 0
改变 n/4 n/2 n n/4
平衡 n/4 n/2 n n/4
混合气体的密度=(nMA/2+NMB)/(n/2+n+n/4)V=( nMA/2+NMB)/(7nV/4),根据气体密度公式分析,气体的密度与加入B的多少无关,所以若再加入B ,则再次达到平衡,反应体系中气体密度始终不变,错误,不选C;D、根据图像结合方程式可知,加入B的物质的量与生成C的物质的量相等,所以该反应中有一半的B反应,所以其转化率为50%,正确,选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目