题目内容
在一定温度下,在恒定容积的密闭容器中进行的可逆反应A2(g)+B2(g) 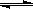 2AB(g)达到化学平衡的标志是
2AB(g)达到化学平衡的标志是
A.容器内的总压强不随时间而变化
B.反应速率v(A2) =v(B2)= 1/2v(AB)
C.单位时间内有n molA2生成的同时就有2n molAB生成
D.容器内混合气体的密度不随时间而变化
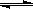 2AB(g)达到化学平衡的标志是
2AB(g)达到化学平衡的标志是A.容器内的总压强不随时间而变化
B.反应速率v(A2) =v(B2)= 1/2v(AB)
C.单位时间内有n molA2生成的同时就有2n molAB生成
D.容器内混合气体的密度不随时间而变化
C
在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。反应前后体积不变,所以压强始终也是不变的,A不正确。速率之比是相应的化学计量数之比,因此B中的关系始终是成立,不正确。C中反应速率的方向相反,且满足速率之比是相应的化学计量数之比,正确。密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,D不正确。混答案选C。

练习册系列答案
相关题目
 CH3OH(g) ΔH1
CH3OH(g) ΔH1 a、容器各物质的浓度保持不变; b、容器内压强保持不变;
a、容器各物质的浓度保持不变; b、容器内压强保持不变;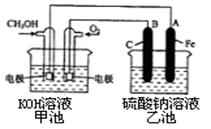
 2CO2+N2,其部分化学平衡常数如下表:
2CO2+N2,其部分化学平衡常数如下表: CO2+1/2N2,则100℃时,K的值= 。
CO2+1/2N2,则100℃时,K的值= 。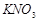 的溶解度s
的溶解度s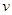
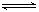 C分别在三种不同实验条件下进行,它们的起始浓度均为
C分别在三种不同实验条件下进行,它们的起始浓度均为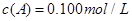 、
、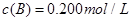 及
及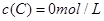 。反应物A的浓度随时间的变化如下图所示。
。反应物A的浓度随时间的变化如下图所示。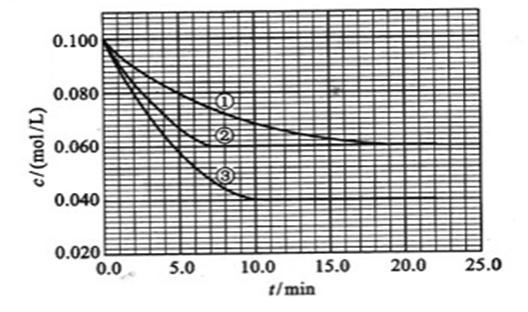
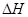 _________0,判断其理由是__________ __
_________0,判断其理由是__________ __  2SO3(g)△H =-a kJ·mol-1。在相同条件下,要想得到2a kJ的热量,加入各物质的物质的量可能是( )
2SO3(g)△H =-a kJ·mol-1。在相同条件下,要想得到2a kJ的热量,加入各物质的物质的量可能是( ) (g)+W(s) ΔH>0一段时间后,达到化学平衡状态.下列叙述正确的是
(g)+W(s) ΔH>0一段时间后,达到化学平衡状态.下列叙述正确的是 N2O4(g)反应达平衡后,保持其它条件不变,压缩混合气体体积,所观察到的现象是( )
N2O4(g)反应达平衡后,保持其它条件不变,压缩混合气体体积,所观察到的现象是( ) 2Q(g) + nR(g),反应达平衡后,容器内压强比原来增加5%,X的浓度减少1/3,则n值可能为
2Q(g) + nR(g),反应达平衡后,容器内压强比原来增加5%,X的浓度减少1/3,则n值可能为