题目内容
17.合理应用和处理氮的化合物,在生产生活中有重要意义.(1)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料.
①以尿素为原料在一定条件下发生反应:CO(NH2)2 (s)+H2O(l)?2NH3(g)+CO2(g)?△H=+133.6kJ/mol.该反应的化学平衡常数的表达式K=c2(NH3)•c(CO2).关于该反应的下列说法正确的是a(填序号).
a.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b.在平衡体系中增加水的用量可使该反应的平衡常数增大
c.降低温度使尿素的转化率增大
②尿素在一定条件下可将氮的氧化物还原为氮气.
结合①中信息,尿素还原NO(g)的热化学方程式是2CO(NH2)2(s)+6NO(g)=5N2(g)+2CO2(g)+4H2O(l)△H=-1804.7KJ/mol.
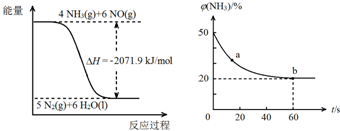
③密闭容器中以等物质的量的NH3和CO2为原料,在120℃、催化剂作用下反应生成尿素:CO2(g)+2NH3(g)═CO (NH2)2 (s)+H2O(g),混合气体中NH3的物质的量百分含量[ϕ(NH3)]随时间变化关系如图所示.则a点的正反应速率ν(正)(CO2)>b点的逆反应速率ν(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是75%.
(2)NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2.已知9.2g NO2和Na2CO3溶液完全反应时转移电子0.1mol,此反应的离子方程式是2NO2+CO32-=NO3-+NO2-+CO2;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中离子浓度大小关系是c(Na+)>c(NO3-)>c(NO2-)>c(OH-)>c(H+).
分析 (1)①化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
a.混合气体中只有氨气、二氧化碳,二者物质的量之比为定值2:1,平均相对分子质量不变;
b.平衡常数只受温度影响;
c.正反应为吸热反应,降低温度平衡逆向移动;
②尿素在一定条件下可将氮的氧化物还原为氮气,反应方程式为:2 CO(NH2)2(s)+6 NO(g)=5 N2(g)+2CO2(g)+4 H2O(l),
已知:①CO(NH2)2 (s)+H2O(l)?2NH3(g)+CO2(g)?△H=+133.6kJ/mol,
由图可得热化学方程式:②4NH3(g)+6 NO(g)=5 N2(g)+6H2O(l)△H=-2071.9 kJ/mol,
根据盖斯定律,①×2+②可得:2 CO(NH2)2(s)+6 NO(g)=5 N2(g)+2CO2(g)+4 H2O(l);
③a点未到达平衡,反应继续向正反应进行,正反应速率减小、逆反应速率增大到b点平衡状态时正逆速率相等;
设NH3和CO2的起始物质的量为1mol,平衡时氨气转化率为x,表示出平衡时各组分物质的量,结合氨气的体积分数20%列方程计算;
(2)9.2gNO2的物质的量$\frac{9.2g}{46g/mol}$=0.2mol,Na2CO3溶液完全反应生成CO2时转移电子0.1mol,反应中只有N元素化合价变化,则N的化合价分别由+4价变化为+5价和+3价,反应的离子方程式为:2NO2+CO32-=NO3-+NO2-+CO2,在碱性溶液中应生成NaNO3和NaNO2,二者浓度相等,NO2-水解溶液呈碱性.
解答 解:(1)①化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出,CO(NH2)2 (s)+H2O(l)?2NH3(g)+CO2(g)平衡常数K=c2(NH3)•c(CO2);
a.混合气体中只有氨气、二氧化碳,二者物质的量之比为定值2:1,平均相对分子质量不变,故a正确;
b.平衡常数只受温度影响,温度不变,平衡常数不变,增加水的用量不影响平衡常数,故b错误;
c.正反应为吸热反应,降低温度平衡逆向移动,尿素的转化率减小,故c错误,
故答案为:c2(NH3)•c(CO2);a;
②尿素在一定条件下可将氮的氧化物还原为氮气,反应方程式为:2 CO(NH2)2(s)+6 NO(g)=5 N2(g)+2CO2(g)+4 H2O(l),
已知:①CO(NH2)2 (s)+H2O(l)?2NH3(g)+CO2(g)?△H=+133.6kJ/mol,
由图可得热化学方程式:②4NH3(g)+6 NO(g)=5 N2(g)+6H2O(l)△H=-2071.9 kJ/mol,
根据盖斯定律,①×2+②可得:2CO(NH2)2(s)+6NO(g)=5N2(g)+2CO2(g)+4H2O(l)△H=-1804.7KJ/mol,
故答案为:2CO(NH2)2(s)+6NO(g)=5N2(g)+2CO2(g)+4H2O(l)△H=-1804.7KJ/mol;
③氨气的体积分数从50%变化为20%后体积分数保持不变,说明b点反应达到平衡状态,a点氨气体积百分含量大于b的氨气体积百分含量,说明反应正向进行达到平衡状态,a点的正反应速率大于b点的正反应速率,故v正(CO2)>v逆(CO2);
设NH3和CO2的起始物质的量为1mol,平衡时氨气转化率为x,则:
CO2(g)+2NH3(g)?CO (NH2)2 (s)+H2O(g),
起始量(mol):1 1 0
变化量(mol):0.5x x 0.5x
平衡量(mol):1-0.5x 1-x 0.5x
氨气的体积分数=$\frac{1-x}{2-x}$=20%,解得x=75%,
故答案为:>;75%;
(2)9.2gNO2的物质的量$\frac{9.2g}{46g/mol}$=0.2mol,Na2CO3溶液完全反应生成CO2时转移电子0.1mol,反应中只有N元素化合价变化,则N的化合价分别由+4价变化为+5价和+3价,反应的离子方程式为:2NO2+CO32-=NO3-+NO2-+CO2,在碱性溶液中应生成NaNO3和NaNO2,二者浓度相等,NO2-水解溶液呈碱性,所得溶液中的离子浓度大小关系为c(Na+)>c(NO3-)>c(NO2-)>c(OH-)>c(H+),
故答案为:2NO2+CO32-=NO3-+NO2-+CO2;c(NO3-)>c(NO2-)>c(OH-)>c(H+).
点评 本题考查盖斯定律应用、化学平衡计算、平衡常数、离子浓度大小比较等,是对学生综合能力的考查,难度中等.

| A. | Na+ K+ OH- Cl- | B. | Na+ Fe3+ SO42- NO3- | ||
| C. | Mg2+ Na+ SO42- Cl- | D. | Ba2+ HCO3- NO3- K+ |
| A. | 已知C2H6的燃烧热为1090 kJ•mol-1,则C2H6燃烧的热化学方程式为:C2H6(g)+3.5O2(g)═2CO2(g)+3H2O(g)△H=-1090 kJ/mol | |
| B. | 25℃,101kPa下,l mol C6H6燃烧生成CO2和液态水时放出3260 kJ热量,其热化学方程式为:C6H6(g)+7.5O2(g)═6CO2(g)+3H2O (l)△H=-3260kJ•mol-1 | |
| C. | 已知常温下:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,则稀醋酸与稀NaOH溶液反应生成1 mol H2O(l)时也放出57.3 kJ的热量 | |
| D. | 已知2CO(g)+O2(g)═2CO2(g)△H=-566 kJ•mol-1,则CO的燃烧热△H=-283 kJ•mol-1 |
 为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过下列反应,使CCl4转化为重要的化工原料氯仿(CHCl3).CCl4+H2?CHCl3+HCl此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4等.已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃.
为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过下列反应,使CCl4转化为重要的化工原料氯仿(CHCl3).CCl4+H2?CHCl3+HCl此反应伴随有副反应,会生成CH2Cl2、CH3Cl和CH4等.已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃.在密闭容器中,该反应达到平衡后,测得如下数据(假设不考虑副反应).
| 实验 序号 | 温度℃ | 初始CCl4浓度 (mol•L-1) | 初始H2浓度(mol•L-1) | CCl4的平衡转化率 |
| 1 | 110 | 1 | 1.2 | A |
| 2 | 110 | 1 | 1 | 50% |
| 3 | 100 | 1 | 1 | B |
(2)实验l中,CCl4的转化率A大于50%(填“大于”、“小于”或“等于”).
(3)实验3中,B的值D(选填序号).
A.等于50% B.大于50% C.小于50% D.从本题资料,无法判断
(4)120℃,在相同条件的密闭容器中,分别进行H2的初始浓度为2mol•L-1和4mol•L-1的实验,测得反应消耗CCl4的百分率(x%)和生成物中CHCl3,的百分含量(y%)随时间(t)的变化关系如图(图中实线是消耗CCl4的百分率变化曲线,虚线是产物中CHCl3的百分含量变化曲线).在图中的四条线中,表示H2起始浓度为2mol•L一1实验的消耗CCl4的百分率变化曲线是③(选填序号).
| A. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=-48.40kJ•mol-1 | |
| B. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2 (g)+9H2O(l)△H=-5517.60kJ•mol-1 | |
| C. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(g)△H=-5517.60kJ•mol-1 | |
| D. | 2C8H18(l)+25O2(g)═16CO2 (g)+18H2O(l)△H=-11035.20kJ•mol-1 |
| A. | H(g)+Cl(g)═HCl(g)△H=-431kJ•mol-1 | |
| B. | 2HCl(g)═H2(g)+Cl2(g)的反应热△H<0 | |
| C. | H2(g)+Cl2(g)═2HCl(g)△H=-183kJ | |
| D. | 相同条件下,H2(g)+Cl2(g)═2HCl(g)反应在光照和点燃条件下的△H不相等 |
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1mol A2、3mol B2 | 2mol AB3 | 2mol AB3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应的平衡常数K | K甲 | K乙 | K丙 |
| 平衡时AB3的浓度/mol•L-1 | c甲 | c乙 | c丙 |
| 平衡时AB3的反应速率/mol•L-1•min-1 | v甲 | v乙 | v |
| A. | v甲=v丙 | B. | c乙>c甲 | C. | V甲>V丙 | D. | K乙<K丙 |
| A. | 质量是 4 g | B. | 体积是 33.6 L | ||
| C. | 电子数是3 | D. | 分子数约为 1.5×6.02×1023 个 |