题目内容
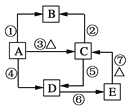
【题目】关于下列各装置图的叙述不正确的是

A. 用图①装置实现铁上镀铜,a 极为铜,电解质溶液可以是CuSO4溶液
B. 图②装置盐桥中 KCl的 Cl-移向乙烧杯
C. 图③装置中钢闸门应与外接电源的负极相连获得保护
D. 图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同
【答案】B
【解析】
A用图①装置实现铁上镀铜,根据电流方向知a为电解池的阳极失电子,b为电解池的阴极的电子,要实现铁上镀铜,a 极为铜,b极为铁,电极电解质溶液可以是CuSO4溶液。故A项说法正确;B图②装置是原电池,甲电极为锌原电池的负,极反应:![]() ,乙电极为铜,做原电池的正极得电子,正极反应为:
,乙电极为铜,做原电池的正极得电子,正极反应为:![]() ,在反应过程中,氯离子起到传导电子的作用,则其应该移向负极,也就是甲烧杯,故B项错误; C项,此反应的目的是保护钢闸门不受腐蚀,因此钢闸门应该连在电源的阴极,发生还原反应才能够达到这个目的,故C项正确;D项,左边装置的负极反应方程式:
,在反应过程中,氯离子起到传导电子的作用,则其应该移向负极,也就是甲烧杯,故B项错误; C项,此反应的目的是保护钢闸门不受腐蚀,因此钢闸门应该连在电源的阴极,发生还原反应才能够达到这个目的,故C项正确;D项,左边装置的负极反应方程式:![]() ,右边装置的负极反应式:
,右边装置的负极反应式:![]() ,这两个装置中通过相同数目的电子时,消耗的负极材料的物质的量之比应该为2:3,故D项正确。
,这两个装置中通过相同数目的电子时,消耗的负极材料的物质的量之比应该为2:3,故D项正确。
综上所述,本题正确答案为B。

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目