题目内容
写出下列物质溶于水时的电离方程式
(1)硫酸铵 .(2)氧氧化钡 .
(1)硫酸铵
分析:强电解质的电离不可逆,用“═”,弱电解质的电离可逆,用“?”.
解答:解:(1)铵盐均属于可溶性的强电解质,所以硫酸铵的电离方程式应为(NH4)2SO4 =2NH4++SO42-,故答案为:(NH4)2SO4 =2NH4++SO42-;
(2)氢氧化钡是强碱,属于强电解质,所以氢氧化钡的电离方程式应为Ba(OH)2=Ba2++2OH-,故答案为:Ba(OH)2=Ba2++2OH-.
(2)氢氧化钡是强碱,属于强电解质,所以氢氧化钡的电离方程式应为Ba(OH)2=Ba2++2OH-,故答案为:Ba(OH)2=Ba2++2OH-.
点评:本题考查学生电离方程式的书写方法,可以根据所学知识进行回答,较简单.

练习册系列答案
相关题目
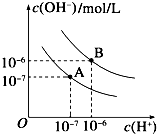 (1)写出下列物质溶于水的电离方程式①冰醋酸溶于水:
(1)写出下列物质溶于水的电离方程式①冰醋酸溶于水: