题目内容
【题目】瑞典ASES公司设计的曾用于驱动潜艇的液氨﹣液氧燃料电池示意图如图所示,下列有关说法正确的是( ) 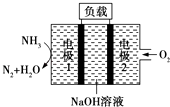
A.电池工作时,Na+向电极1移动
B.电池工作一段时间后停止,溶液PH值比开始时明显减小
C.电极1发生的电极反应为2NH3+6OH﹣﹣6e﹣═N2↑+6H2O
D.用该电池做电源电解精炼铜,理论上每消耗0.2 mol NH3的同时阳极会得到19.2g纯铜
【答案】BC
【解析】解:A.1为负极,原电池工作时,阳离子向正极移动,故A错误; B.总方程式为4NH3+3O2=2N2+6H2O,生成水,溶液体积增大,pH减小,故B正确;
C.在燃料电池的负极上发生燃料氨气失电子的氧化反应,则碱性环境下电极1发生的电极反应为:2NH3+6OH﹣﹣6e﹣=N2↑+6H2O,故C正确;
D.由2NH3+6OH﹣﹣6e﹣=N2↑+6H2O可知,理论上每消耗0.2 mol NH3 , 可转移0.6mol电子,但阳极不是纯铜,阳极发生氧化反应,故D错误.
故选BC.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
