题目内容
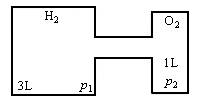
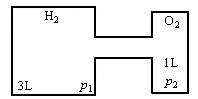
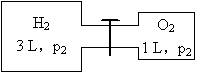
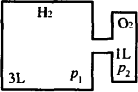
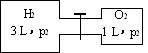
在10℃时,有体积为3 L和1 L的容器,如下图所示。图中左、右两容器内分别充入氢气和氧气,压力各为p1和p2,开启阀门,点燃,反应后将气体冷却至原温度,计算:
(1)在10℃时反应前在p1下氧气的体积。
(2)在10℃时反应后容器的压力p。
答案:
解析:
提示:
解析:
(1)V=
|
提示:
(1)p1×V=p2×1 L,V=p2/p1 L; (2)n(H 当n(H2)>2n(O2)时,剩余H2,其物质的量为(3p1-2p2)/RT。p×4={(3p1-2p2)/RT}×RT解得p=(3p1-2p2)/4。 当n(H2)=2n(O2)时,无气体剩余,p=0。 当n(H2)<2n(O2)时,剩余O2,其物质的量为(p2-3p1/2)/RT,p×4={(p2-3p1/2)/RT }×RT,解得p=(p2-1.5p1)/4。
|

练习册系列答案
相关题目