题目内容
盐酸、硫酸和硝酸是中学阶段常见的三种酸.请就三种酸与金属铜反应的情况,回答下列问题:(1)稀盐酸与铜不反应,但向稀盐酸中加入H2O2后,则可使铜溶解,该反应的离子方程式为______.
某同学未加入氧化剂,而是设计了一个实验装置,也能使铜很快溶于稀盐酸.请在方格中画出该装置

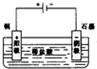
(2)由4根同质量的电极材料(Ag Cu Pt)组成下列装置.下列装置A为______池(填写”原电”或”电解”),发生氧化反应的电极反应式为:______,B池中阳极的电极反应式为:______.当关闭电键k一段时间,发现Ag棒与 Cu棒质量差为28g时,则装置B产生气体的总质量为______g(电解质溶液足量).

(3)将等质量的铜片分别与等体积、过量的浓硝酸和稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出可能是Cu2+浓度不同引起的,你同意这种看法吗?______(填“同意”或“不同意”),理由是______.
某同学未加入氧化剂,而是设计了一个实验装置,也能使铜很快溶于稀盐酸.请在方格中画出该装置

(2)由4根同质量的电极材料(Ag Cu Pt)组成下列装置.下列装置A为______池(填写”原电”或”电解”),发生氧化反应的电极反应式为:______,B池中阳极的电极反应式为:______.当关闭电键k一段时间,发现Ag棒与 Cu棒质量差为28g时,则装置B产生气体的总质量为______g(电解质溶液足量).

(3)将等质量的铜片分别与等体积、过量的浓硝酸和稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出可能是Cu2+浓度不同引起的,你同意这种看法吗?______(填“同意”或“不同意”),理由是______.
(1)双氧水具有氧化性,在酸性环境下能将金属铜氧化,离子方程式为:Cu+H2O2+2HCl=CuCl2+2H2O,用电解原理实现铜和盐酸的反应,根据电解原理阳极必须是金属铜,电解质必须是稀盐酸,故答案为:Cu+H2O2+2HCl=CuCl2+2H2O;
(2)根据装置的特点,确定装置A为原电池,装置B为电解池,原电池中,失电子的极为负极,负极发生氧化反应,电极反应为:Cu-2e-=Cu2+,和原电池正极相连的为电解池的阳极,阴离子放电,电极反应为:4OH--4e-=2H2O+O2,当Ag棒与 Cu棒质量差为28g时,设反应转移电子数为x,则Cu棒质量减少32x,Ag棒质量增加108x,所以108x+32x=28,x=0.2mol,装置B中相当于电解水,阳极放氧气的质量为:0.05mol×32g/mol=1.6g,阴极放氢气的质量为0.2g,故装置B产生气体的总质量为1.8g,故答案为:1.8;
(3)将等质量的铜片分别与等体积、过量的浓硝酸和过量的稀硝酸反应后,所得溶液中Cu2+的浓度基本相等,颜色基本相同,故答案为:不同意;等质量的铜片与等体积、过量的浓硝酸、稀硝酸反应,所得溶液中Cu2+的浓度基本相等.

练习册系列答案
相关题目
 盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.现就三大酸与金属铜反应的情况,回答下列问题:
盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.现就三大酸与金属铜反应的情况,回答下列问题:

