题目内容
合成氨工业对化学工业和国防工业具有重要意义。设在容积为2.0 L的密闭容器中充入0.80 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的体积分数为20%。
![]() (1) 该条件下反应2NH3(g)
(1) 该条件下反应2NH3(g)![]() N2(g)+ 3H2(g)的平衡常数为 。
N2(g)+ 3H2(g)的平衡常数为 。
![]() (2)相同条件下,在另一相同容器中充入a mol N2(g)和b mo1 H2(g),达到平衡时,测得容器中NH3为0.8 mol,H2为2.0 mol,则
(2)相同条件下,在另一相同容器中充入a mol N2(g)和b mo1 H2(g),达到平衡时,测得容器中NH3为0.8 mol,H2为2.0 mol,则![]() 。
。
![]() (3)工业上可利用CH4(g)+H2O(g)
(3)工业上可利用CH4(g)+H2O(g)![]() CO(g)+3H2(g)反应生产合成氨原料气H2。已知温度、压强和水碳比[
CO(g)+3H2(g)反应生产合成氨原料气H2。已知温度、压强和水碳比[![]() ]对甲烷蒸汽转化反应的影响如下图:
]对甲烷蒸汽转化反应的影响如下图:
![]()
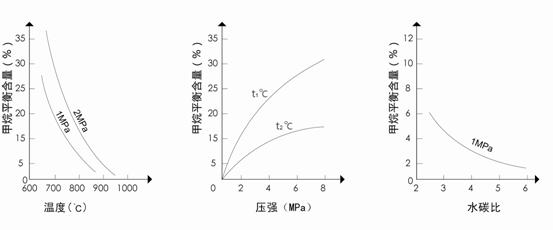
![]() 图1(水碳比为3) 图2(水碳比为3) 图3(800℃)
图1(水碳比为3) 图2(水碳比为3) 图3(800℃)
![]()
![]()
![]() ①降低反应的水碳比平衡常数K__________(选填“增大”、“减小”或“不变”);
①降低反应的水碳比平衡常数K__________(选填“增大”、“减小”或“不变”);![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 升高温度,平衡向____________方向移动(选正反应或逆反应)。
升高温度,平衡向____________方向移动(选正反应或逆反应)。
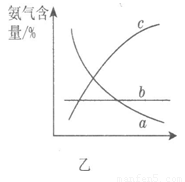
![]() ②图2中,两条曲线所示温度的关系是:t1_____t2(选填>、=或<);
②图2中,两条曲线所示温度的关系是:t1_____t2(选填>、=或<);
![]() 图1中,在800℃、2MPa比1MPa时的甲烷含量_______(选填高、低或不变),
图1中,在800℃、2MPa比1MPa时的甲烷含量_______(选填高、低或不变),
![]()
![]()
![]()
(1)0.9375 (2分) (2)0.7(2分)(3)①不变 (1分) 正反应(1分) ② < (1分) 高(1分)
![]()
![]()

练习册系列答案
相关题目
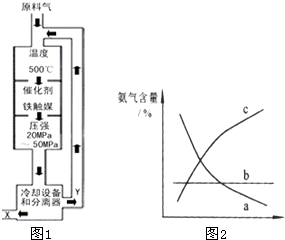 (2008?佛山一模)(1)合成氨工业对化学工业和国防工业具有重要意义.工业合成
(2008?佛山一模)(1)合成氨工业对化学工业和国防工业具有重要意义.工业合成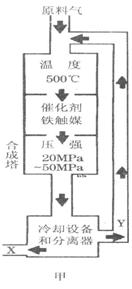
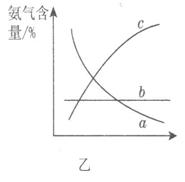
 ②图甲中条件选定的主要原因是(选填字母序号,下同)________。
②图甲中条件选定的主要原因是(选填字母序号,下同)________。 某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
 某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系: