题目内容
下列说法正确的是( )
| A、同主族元素的氢化物中,稳定性最好的其沸点也最高 |
| B、最外层电子数相同的主族元素的原子,化学性质完全相同 |
| C、第三周期非金属元素Si、P、S、Cl的氧化物对应的水化物酸性依次增强 |
| D、同周期IA族元素的金属性比IIA族元素的金属性强 |
考点:元素周期表的结构及其应用,元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.如不含氢键,则核电荷数越大,对应的氢化物沸点越高;
B.同主族元素的单质、化合物具有相似性和递变性;
C.应为最高价氧化物对应的水化物;
D.同周期元素从左到右元素的金属性逐渐减小.
B.同主族元素的单质、化合物具有相似性和递变性;
C.应为最高价氧化物对应的水化物;
D.同周期元素从左到右元素的金属性逐渐减小.
解答:
解:A.非金属性Cl>Br,稳定性HCl>HBr,但沸点HCl<HBr,故A错误;
B.同主族元素的单质、化合物具有相似性和递变性,化学性质不一定完全相同,如氟气和水反应生成氧气,氯气和水反应生成盐酸和次氯酸,没有氧气生成,故B错误;
C.应为最高价氧化物对应的水化物,故C错误;
D.同周期元素从左到右元素的金属性逐渐减小,则同周期IA族元素的金属性比IIA族元素的金属性强,故D正确.
故选D.
B.同主族元素的单质、化合物具有相似性和递变性,化学性质不一定完全相同,如氟气和水反应生成氧气,氯气和水反应生成盐酸和次氯酸,没有氧气生成,故B错误;
C.应为最高价氧化物对应的水化物,故C错误;
D.同周期元素从左到右元素的金属性逐渐减小,则同周期IA族元素的金属性比IIA族元素的金属性强,故D正确.
故选D.
点评:本题考查较为综合,涉及元素周期律、周期表等知识,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意把握元素周期律的递变规律以及相关基础知识的积累,难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A、3.4g NH3中含N-H键数目为0.2NA |
| B、1L 0.1mol?L-1 HClO溶液中H+数为0.1NA |
| C、标准状况下,22.4L C2H5OH中含有的氢原子数为6NA |
| D、常温常压下,92g的NO2和N2O4混合气体含有的原子总数为6NA |
设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、在密闭容器中,使1mol N2与3mol H2充分反应后生成NH3的分子数为2NA |
| B、标准状况下,4.48L N2中含有的共用电子对数为0.2NA |
| C、常温常压下,1mol NaHSO4晶体中含有的离子总数为2NA |
| D、标准状况下,1mol Fe与2.24L Cl2完全反应后转移的电子数为3NA |
设NA为阿伏加德罗常数值,下列叙述中不正确的是( )
| A、12.4g白磷晶体中含有的P-P键数是0.6NA |
| B、2.9g熟石膏2CaSO4?H2O 含有的结晶水分子数为0.02NA |
| C、100g的98%的浓 H2SO4中所含的硫原子数为NA |
| D、2mol SO2和1mol O2混合在一定条件下密闭容器中加热反应后,容器内物质分子数大于2NA |
下列有关阿佛加德罗常数(NA)的说法错误的是( )
| A、22.4L H2所含的分子数目为NA |
| B、18g H2O含有的H2O分子数目为NA |
| C、0.5mol H2O含有的原子数目为1.5NA |
| D、2NA个氯气分子的物质的量是2mol |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下,6g二氧化硅含有Si-O键数目为2NA |
| B、54克Al与氢氧化钠反应产生气体67.2L |
| C、Na与足量O2反应生成1mol Na2O或1mol Na2O2均失去2NA电子 |
| D、各5.6g铁分别与足量的盐酸反应,电子转移总数均为0.3NA |
下列说法错误的是( )
| A、ⅠA族都是活泼的金属元素 |
| B、ⅡA族元素形成的单质常温下都是固体 |
| C、ⅣA族既有金属元素,也有非金属元素 |
| D、ⅦA族元素形成的单质中,常温下有气、固、液三种状态低 |
下列与化学实验有关的说法正确的是( )
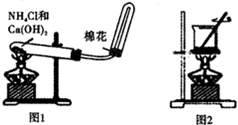

| A、用洁净的铂丝蘸取溶液在火焰上灼烧,产生黄色火焰,则该溶液中一定不含K+ |
| B、将氯水点到蓝色石蕊试纸上,试纸接触点先变红后褪色,说明氯水中含H+具有酸性,含Cl2而具有漂白性 |
| C、如图1装置可用于实验室制备氨气 |
| D、如图2装置可灼烧海带成灰 |
已知CaH2中Ca为+2价,对于CaH2+2H2O═Ca(OH)2+2H2↑,下列说法正确的是( )
| A、H2都是还原产物 |
| B、H2都是氧化产物 |
| C、CaH2中的氢元素既被氧化又被还原 |
| D、氧化产物与还原产物的质量比为1:1 |