题目内容
13.下列关于主族元素的说法正确的是( )| A. | 主族元素的原子核外电子最后填入的能级是s能级 | |
| B. | 主族元素的原子核外电子最后填入的能级是s能级或p能级 | |
| C. | 主族元素的最高正价等于主族的序数 | |
| D. | 主族元素的价电子数有可能超过最外层电子数 |
分析 A、主族元素原子的外围电子排布为nsx、ns2npy(零族元素除外);
B、主族元素原子的外围电子排布为nsx、ns2npy(零族元素除外);
C、氟元素、氧元素没有正化合价;
D、主族元素的最外层电子数为价电子数.
解答 解:A、主族元素原子的外围电子排布为nsx、ns2npy(零族元素除外),故主族元素的原子核外电子最后填入的能级是s能级或p能级,故A错误;
B、主族元素原子的外围电子排布为nsx、ns2npy(零族元素除外),故主族元素的原子核外电子最后填入的能级是s能级或p能级,故B正确;
C、氟元素、氧元素没有正化合价,故C错误;
D、主族元素的最外层电子数等于其价电子数,故D错误;
故选B.
点评 本题考查结构性质关系、主族元素电子排布特征等,难度不大,注意整体把握元素周期表.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.下列实验操作可以达到实验目的是( )
| 实验目的 | 实验操作 | |
| A | 检验工业废水中是否含有苯酚 | 在试管中加入2 mL工业废水样品,然后加入2滴浓溴水,振荡,观察是否产生白色沉淀 |
| B | 验证乙醛中含有醛基 | 在试管中加入2 mL10%的CuSO4溶液,然后加入4至6滴2%的NaOH溶液振荡,再加入0.5 mL乙醛溶液加热煮沸,观察是否出现红色沉淀 |
| C | 提纯粗苯甲酸 | 将1g粗苯甲酸溶于50mL蒸馏水,加热使之全部溶解,趁热过滤,将滤液冷却结晶,滤出晶体 |
| D | 证明溴乙烷发生消去反应生成乙烯 | 将产生的气体通入酸性高锰酸钾溶液中,观察溶液是否褪色 |
| A. | A | B. | B | C. | C | D. | D |
4.下列关于原子的几种描述中,正确的是( )
| A. | 硫的原子结构示意图: | |
| B. | Be2+离子中的质子数和电子数之比为2:1 | |
| C. | 原子核内有8个中子的碳原子:${\;}_{8}^{14}$C | |
| D. | 同一元素的各种同位素的物理性质、化学性质均相同 |
1.(1)在配合物[Fe(SCN)]2+中,提供空轨道接受孤对电子的微粒是Fe3+,画出配合物离子[Cu(NH3)4]2+中的配位键 .
.
(2)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式:(各写一种)正四面体分子CH4或CF4,三角锥形分子NH3或NF3,V形分子H2O.
(3)按要求填写下表中有序号的空格:
 .
.(2)按要求写出由第二周期元素为中心原子,通过sp3杂化形成中性分子的化学式:(各写一种)正四面体分子CH4或CF4,三角锥形分子NH3或NF3,V形分子H2O.
(3)按要求填写下表中有序号的空格:
| 元素符号 | 电子排布式 | 价层电子排布 | 在周期表中的位置 |
| ① | 1s22s22p6 | ② | ③ |
| Cr | ④ | ⑤ | ⑥ |
8.室温下,同种规格的铝片分别与下列物质混合,产生氢气速率最大的是( )
| A. | 0.1 mol/L的盐酸15mL | B. | 0.15 mol/L 的硫酸溶液8mL | ||
| C. | 0.2 mol/L 的盐酸12mL | D. | 18 mol/L的浓硫酸15mL |
18.关于元素周期表,下列叙述中不正确的是( )
| A. | IA族元素称为碱金属元素 | |
| B. | 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素 | |
| C. | 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 | |
| D. | 地球上元素的分布和它们在元素周期表中的位置有密切关系 |
3.同周期的X、Y、Z三种元素,已知其氢化物分别为XH3、H2Y、HZ,则下列判断正确的是( )
| A. | 原子半径 Z>Y>X | |
| B. | Z的非金属性最强 | |
| C. | 氢化物还原性XH3>H2Y>HZ,稳定性XH3>H2Y>HZ | |
| D. | 最高氧化物对应水化物H3XO4酸性最强 |
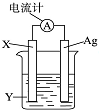 依据氧化还原反应:2Ag++Cu═Cu2++2Ag设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag++Cu═Cu2++2Ag设计的原电池如图所示.请回答下列问题: 能源是现代社会发展的支柱之一,化学能是重要的能源.
能源是现代社会发展的支柱之一,化学能是重要的能源.