题目内容
 mol N2含有x个N2,则阿伏加德罗常数为( )。
mol N2含有x个N2,则阿伏加德罗常数为( )。A.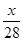 | B.14x mol-1 | C.28x mol-1 | D.28x |
C
试题分析:
 mol N2含有x个N2,则1 mol N2含有28x个N2,即阿伏加德罗常数。
mol N2含有x个N2,则1 mol N2含有28x个N2,即阿伏加德罗常数。
练习册系列答案
相关题目
题目内容
 mol N2含有x个N2,则阿伏加德罗常数为( )。
mol N2含有x个N2,则阿伏加德罗常数为( )。A.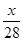 | B.14x mol-1 | C.28x mol-1 | D.28x |
 mol N2含有x个N2,则1 mol N2含有28x个N2,即阿伏加德罗常数。
mol N2含有x个N2,则1 mol N2含有28x个N2,即阿伏加德罗常数。