题目内容
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
CO(g) +H2O(g)  CO2(g) +H2 (g) △H<0。
CO2(g) +H2 (g) △H<0。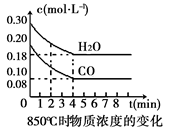
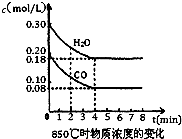
(1)CO和H2O浓度变化如上图,则在该温度下,该反应的平衡常数K= 。
0~4min的平均反应速率v(CO)=_____mol·L-1·min-1。若降低温度,该反应的K值将 ,该反应的化学反应速率将 (填“增大”“减小”或“不变”)。
(2)在相同容器中发生上述反应,当温度高于850℃时,
容器内各物质的浓度变化如下表。
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 | |
①表中3min~4min之间反应处于_________状态; c 1数值_________0.08 mol·L-1 (填大于、小于或等于)。
②反应在4min~5min间,平衡向逆方向移动,可能的原因是_________
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度
(3)在相同温度下(850℃),若起始时c(CO)=1mol·L-1,c(H2O)=2mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,则此时该反应是否达到平衡状态 (填“是”与“否”),此时v(正) v(逆)(填“大于”“小于”或“等于”),你判断的依据是 。
(1)1 (2分)0.03(2分) 增大(1分) 减小(1分)
(2)①平衡(1分) 大于(1分)②d (2分)
(3)否、(1分)大于(1分) 因为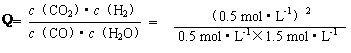
=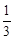 <K,反应向右进行。(2分)
<K,反应向右进行。(2分)
解析试题分析:(1)由图可以知道CO和H2O浓度在达到平衡时的浓度分别为0.08、0.18mol/L,反应生成的CO2、H2都为0.12mol/L,则在该温度下,该反应的平衡常数
K=0.12×0.12/(0.08×0.18)=1;0~4min的平均反应速率v(CO)=(0.20-0.08)/4=0.03mol·L-1·min-1,△H<0,说明该反应为放热反应,所以降低温度,该反应的K值将增大,温度降低,化学反应速率减小;(2)因为3min~4min各物质的浓度相等,所以3min~4min之间反应处于平衡状态,c 1数值大于0.08 mol·L-1,因为前两分钟的CO化学反应速率为(0.200-0.138)/2=0.031mol·L-1·min-1,根据一个反应浓度减少,化学反应速率也减少,若c 1数值的数值为0.08 mol·L-1,则其在2-3min的平均化学速率为(0.138-0.08)/1=0.058mol·L-1·min-1,这种情况是不可能发生的,所以c 1数值大于0.08 mol·L-1;②反应在4min~5min间,平衡向逆方向移动,可能的原因是为增加氢气浓度,因为产物的浓度均增大,而反应物之一的CO的浓度减少,所以增加氢气浓度,故本题的答案选择d;(3)在相同温度下(850℃),平衡常数为1,因为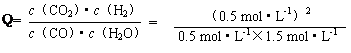
=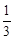 <K=1,所以该反应未达到化学平衡,此时v(正)大于v(逆)。
<K=1,所以该反应未达到化学平衡,此时v(正)大于v(逆)。
考点:化学平衡,化学平衡常数的计算
点评:本题考查了化学平衡,化学平衡常数的计算,这些知识点是高考命题的重点和热点,本题难度适中。

 已知反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,生成的CO2与H2以不同的体积比混合时在合适条件下的反应可制得CH4.
已知反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,生成的CO2与H2以不同的体积比混合时在合适条件下的反应可制得CH4. ,恒容时,温度升高.H2浓度减小。分析下列问题:
,恒容时,温度升高.H2浓度减小。分析下列问题:
 CO+H2O (g),t时刻容器内各物质的浓度分别为:一氧化碳0.09 mol/L、水蒸气0.09 mol/L、二氧化碳0.08 mol/L、氢气 0.08 mol/L,此时v(正) v(逆)(“大于”“ 小于”“等于”)
CO+H2O (g),t时刻容器内各物质的浓度分别为:一氧化碳0.09 mol/L、水蒸气0.09 mol/L、二氧化碳0.08 mol/L、氢气 0.08 mol/L,此时v(正) v(逆)(“大于”“ 小于”“等于”) ,恒容时,温度升高H2浓度减小。试回答
,恒容时,温度升高H2浓度减小。试回答 下列问题:
下列问题: 常数的值K=
常数的值K= 
 CO+H2O (g),t时刻容器内各物质的浓度分别为:一氧化碳0.09 mol/L、水蒸气0.09 mol/L、 二氧化碳0.08 mol/L、氢气 0.08
CO+H2O (g),t时刻容器内各物质的浓度分别为:一氧化碳0.09 mol/L、水蒸气0.09 mol/L、 二氧化碳0.08 mol/L、氢气 0.08 ,恒容时,温度升高H2浓度减小。试回答下列问题:
,恒容时,温度升高H2浓度减小。试回答下列问题:
 CO+H2O (g),t时刻容器内各物质的浓度分别为:一氧化碳0.09 mol/L、水蒸气0.09
mol/L、 二氧化碳0.08 mol/L、氢气 0.08 mol/L,此时v(正)
v(逆)(“大于”“ 小于”或“等于”)
CO+H2O (g),t时刻容器内各物质的浓度分别为:一氧化碳0.09 mol/L、水蒸气0.09
mol/L、 二氧化碳0.08 mol/L、氢气 0.08 mol/L,此时v(正)
v(逆)(“大于”“ 小于”或“等于”)