题目内容
(13分)
(1)1.5molH2SO4的质量是______g,其中含有_____mol H,含有_______g氧元素。
(2)9.03×1023个氨(NH3)分子含___________mol氨分子,____________mol氢原子,________mol质子,________________个电子。
(3)硫酸铝的化学式为___________,0.2mol硫酸铝中有______molAl3+,__ 个SO42-。
(4)0.5mol H2O与_________g硫酸所含的分子数相等,它们所含氧原子数之比是_________,其中氢原子数之比是_________。
(1)1.5molH2SO4的质量是______g,其中含有_____mol H,含有_______g氧元素。
(2)9.03×1023个氨(NH3)分子含___________mol氨分子,____________mol氢原子,________mol质子,________________个电子。
(3)硫酸铝的化学式为___________,0.2mol硫酸铝中有______molAl3+,__ 个SO42-。
(4)0.5mol H2O与_________g硫酸所含的分子数相等,它们所含氧原子数之比是_________,其中氢原子数之比是_________。
(1)147、 3、 96 (2)1.5 、 4.5、 15、 9.03×1024
(3)Al2(SO4)3 、0.4 3.612×1023(4)49、 1:4、 1:1
(3)Al2(SO4)3 、0.4 3.612×1023(4)49、 1:4、 1:1
考查物质的量的有关计算
(1)硫酸的摩尔质量是98g/mol,所以1.5molH2SO4的质量是1.5mol×98g/mol=147g。其中含有3mol氢原子,6mol氧原子,氧原子的摩尔质量是16g/mol,所以氧原子的质量是96g。
(2)根据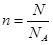 可知,9.03×1023个氨(NH3)分子的物质的量是9.03×1023÷6.02×1023/mol=1.5mol;其中含有4.5mol氢原子。氨气分子中含有10个质子和10个电子,所以含有的质子是15mol,电子数15mol×6.02×1023/mol=9.03×1024。
可知,9.03×1023个氨(NH3)分子的物质的量是9.03×1023÷6.02×1023/mol=1.5mol;其中含有4.5mol氢原子。氨气分子中含有10个质子和10个电子,所以含有的质子是15mol,电子数15mol×6.02×1023/mol=9.03×1024。
(3)硫酸铝的化学式为Al2(SO4)3,所以0.2mol硫酸铝中有0.4molAl3+,0.6mol×6.02×1023/mol=3.612×1023个SO42-。
(4)0.5mol硫酸的质量是0.5mol×98g/mol=49g。根据二者的化学式可知,在物质的量相等的条件下,它们所含氧原子数之比是1︰4,氢原子是之比是1︰1。
(1)硫酸的摩尔质量是98g/mol,所以1.5molH2SO4的质量是1.5mol×98g/mol=147g。其中含有3mol氢原子,6mol氧原子,氧原子的摩尔质量是16g/mol,所以氧原子的质量是96g。
(2)根据
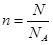 可知,9.03×1023个氨(NH3)分子的物质的量是9.03×1023÷6.02×1023/mol=1.5mol;其中含有4.5mol氢原子。氨气分子中含有10个质子和10个电子,所以含有的质子是15mol,电子数15mol×6.02×1023/mol=9.03×1024。
可知,9.03×1023个氨(NH3)分子的物质的量是9.03×1023÷6.02×1023/mol=1.5mol;其中含有4.5mol氢原子。氨气分子中含有10个质子和10个电子,所以含有的质子是15mol,电子数15mol×6.02×1023/mol=9.03×1024。(3)硫酸铝的化学式为Al2(SO4)3,所以0.2mol硫酸铝中有0.4molAl3+,0.6mol×6.02×1023/mol=3.612×1023个SO42-。
(4)0.5mol硫酸的质量是0.5mol×98g/mol=49g。根据二者的化学式可知,在物质的量相等的条件下,它们所含氧原子数之比是1︰4,氢原子是之比是1︰1。

练习册系列答案
相关题目