题目内容
3.KI溶液中加入稀硫酸和H2O2发生反应:2KI+H2O2+H2SO4═I2+K2S04+2H20,下列关于该反应的说法正确的是( )| A. | H2O2作氧化剂 | B. | H2O2失去电子 | C. | 碘元素被还原 | D. | I-表现氧化性 |
分析 2KI+H2O2+H2SO4═I2+K2S04+2H20,H2O2中氧化合价降低得电子作氧化剂,KI中碘化合价升高作还原剂,据此分析.
解答 解:2KI+H2O2+H2SO4═I2+K2S04+2H20,H2O2中氧化合价降低得电子作氧化剂,KI中碘化合价升高作还原剂,被氧化,表现还原性,则A正确,BCD错误,
故选:A.
点评 本题考查了氧化还原反应的概念分析,抓住氧化还原反应化合价变化是解题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.下列操作使溶液物质的量浓度偏高的是( )
| A. | 没有将洗涤液转移到容量瓶中 | B. | 容量瓶洗净后未经干燥处理 | ||
| C. | 转移过程中有少量的溶液溅出 | D. | 定容时俯视容量瓶刻度线 |
14.实验室需配制一种仅含五种离子(水电离出的离子可忽略)的混合溶液,且在混合溶液中五种离子的物质的量浓度均为1mol/L,下面四个选项中能达到此目的是( )
| A. | Al3+、K+、SO42-、Cl-、AlO2- | B. | Fe2+、H+、Br-、NO3-、Cl- | ||
| C. | Na+、K+、SO42-、NO3-、Cl- | D. | Al3+、Na+、Cl-、SO42-、NO3- |
11.已知某H2SO4、FeSO4、Fe2(SO4)3混合液100mL,其中阳离子浓度相等,SO42-浓度为6mol/L,此溶液中还可溶解铁粉的质量为( )
| A. | 11.2g | B. | 16.8g | C. | 33.6g | D. | 5.6g |
18.下列过程中主要为化学能转化为热能的是( )
| A. |  木柴燃烧 | B. |  光合作用 | C. |  电解冶炼铝 | D. |  风力发电 |
8.将等质量的下列各烃,完全生成CO2和H2O耗氧量最大的是( )
| A. | CH4 | B. | C2H4 | C. | C6H6 | D. | C3H6 |
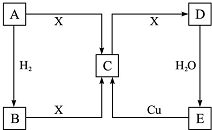 已知A是单质,A、B、C、D、E 5种物质均含同一种元素,X是地壳中含量最多的元素形成的单质,它们的相互转化关系如图所示.试回答下列问题.
已知A是单质,A、B、C、D、E 5种物质均含同一种元素,X是地壳中含量最多的元素形成的单质,它们的相互转化关系如图所示.试回答下列问题. .
. .
.