题目内容
取A、B两份物质的量浓度相等的NaOH溶液.体积均为50ml.分别向其中通入一定量的CO2后,再分别稀释为100 mL.
(1)在NaOH溶液中通入一定量的CO2后.溶液中溶质的组成可能是:
① ② ,③ ④ .
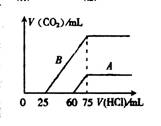
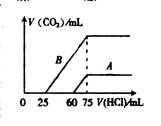
(2)在稀释后的溶液中分别逐滴加0.1 mol/L的盐酸,产生的CO2的体积(标准状况)与所加盐酸的体积关系如图所示:
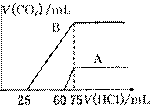
①分别加人足量的盐酸后的溶液中的溶质是 .原NaOH溶液的物质的量浓度为
②A曲线表明.原溶液通入CO2后.所得溶质与HCl反应产生CO2的最大体积是 mL(标准状况).
③B曲线表明,原溶液通入C02后.所得溶质的化学式为
其物质的量之比为 .
(1)NaHCO3 Na2CO3 Na2C03和NaHCO3 Na2C03和NaOH
(2)①NaCl 0.15 mol/L ②33.6 ③Na2C03和NaHCO3 1:1
错解分析:学生不能明确Na2C03和NaHCO3,Na2CO3和NaOH分别与盐酸反应的过程,不能正确理解图像的含义。学生解题时应明确:
Na2C03和NaHCO3与盐酸的反应过程是C032- + H+== HCO3―、HCO3―+ H+= CO2↑+ H2O
Na2CO3和NaOH与盐酸的反应过程是OH- + H+== H2O 、C032- + H+== HCO3―、HCO3―+ H+= CO2↑+ H2O
解题指导:①有图知B溶质为Na2C03和NaHCO3,A溶液溶质为Na2CO3和NaOH,加入足量盐酸生成溶质NaCl,则n(NaCl)==0.075L×0.1mol/L==7.5×10-3mol.n(NaOH)== n(NaCl)==7.5×10-3mol,c(NaOH)== 7.5×10-3mol/0.05L==0.15 mol/L. ②A中产生CO2为0.015L×0.1mol/L==1.5×10-3mol,V(CO2)== 1.5×10-3mol×22.4L/mol==33.6ml. ③B中产生CO2为0.05L×0.1mol/L== 5×10-3mol,V(CO2)==5×10-3mol×22.4L/mol==112ml.

 阅读快车系列答案
阅读快车系列答案 按要求填写下列空白.
按要求填写下列空白.