题目内容
在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
下列说法错误的是( )
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X(g)+3Y(g) 2Z(g),其平衡常数为1 600
2Z(g),其平衡常数为1 600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
| 物质 | X | Y | Z |
| 初始浓度/(mol·L-1) | 0.1 | 0.2 | 0 |
| 平衡浓度/(mol·L-1) | 0.05 | 0.05 | 0.1 |
下列说法错误的是( )
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X(g)+3Y(g)
 2Z(g),其平衡常数为1 600
2Z(g),其平衡常数为1 600C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
C
由 aX + bY  cZ
cZ
初始浓度/(mol·L-1) 0.1 0.2 0
平衡浓度/(mol·L-1) 0.05 0.05 0.1
转化浓度/(mol·L-1) 0.05 0.15 0.1
利用转化浓度之比等于化学计量数之比可得到化学方程式为:X(g)+3Y(g) 2Z(g),这样再利用相关数据可得到A、B正确;D正确,因为平衡常数是温度的函数,C错误。
2Z(g),这样再利用相关数据可得到A、B正确;D正确,因为平衡常数是温度的函数,C错误。
 cZ
cZ初始浓度/(mol·L-1) 0.1 0.2 0
平衡浓度/(mol·L-1) 0.05 0.05 0.1
转化浓度/(mol·L-1) 0.05 0.15 0.1
利用转化浓度之比等于化学计量数之比可得到化学方程式为:X(g)+3Y(g)
 2Z(g),这样再利用相关数据可得到A、B正确;D正确,因为平衡常数是温度的函数,C错误。
2Z(g),这样再利用相关数据可得到A、B正确;D正确,因为平衡常数是温度的函数,C错误。
练习册系列答案
相关题目
 N2(g)+2CO2(g) ΔH=-113.0 kJ/mol,达到平衡后,保持温度不变,缩小容器体积,重新达到平衡后,ΔH变小
N2(g)+2CO2(g) ΔH=-113.0 kJ/mol,达到平衡后,保持温度不变,缩小容器体积,重新达到平衡后,ΔH变小 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则: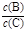 将 。
将 。 Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是( )
Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是( )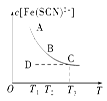
 CH3OH(g)。现在容积均为1 L的a、b、c三个密闭容器中分别充入1 mol CO和2 mol H2的混合气体,控制温度进行反应,测得相关数据的关系如图所示。下列说法正确的是( )
CH3OH(g)。现在容积均为1 L的a、b、c三个密闭容器中分别充入1 mol CO和2 mol H2的混合气体,控制温度进行反应,测得相关数据的关系如图所示。下列说法正确的是( )
 2C(g)(已知反应为放热反应),下列叙述正确的是( )
2C(g)(已知反应为放热反应),下列叙述正确的是( ) 3C(g)+ D(g)在容积不变的密闭容器中进行,达到化学平衡状态的标志是( )
3C(g)+ D(g)在容积不变的密闭容器中进行,达到化学平衡状态的标志是( ) N2O4(无色)的可逆反应中,下列状态一定属于平衡状态的是( )。
N2O4(无色)的可逆反应中,下列状态一定属于平衡状态的是( )。 B(g)+C(g) ΔH=+85.1 kJ·mol-1
B(g)+C(g) ΔH=+85.1 kJ·mol-1