题目内容
【题目】下列有关物质用途的说法中,不正确的是
A. 氢氟酸可用来刻蚀玻瑞 B. 过氧化钠常用作供氧剂
C. 漂白粉可用作游泳池的消毒剂 D. 晶体硅可用于制作光导纤维
【答案】D
【解析】A. 氢氟酸能与二氧化硅反应,可用来刻蚀玻璃,A正确;B. 过氧化钠能与水或二氧化碳反应生成氧气,常用作供氧剂,B正确;C. 漂白粉具有强氧化性,可用作游泳池的消毒剂,C正确;D. 晶体硅可用于半导体,二氧化硅可用于制作光导纤维,D错误,答案选D。

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案【题目】下列实验中,所采取的分离方法与对应原理都正确的是( )
选项 | 目的 | 分离方法 | 原理 |
A | 除去KCl中的MnO2 | 蒸发结晶 | 溶解度不同 |
B | 分离食用油和汽油 | 分液 | 食用油和汽油的密度不同 |
C | 分离KNO3和NaCl | 重结晶 | KN03的溶解度大于NaCl |
D | 除去碘中的NaCl | 加热、升华 | NaCl的熔点高,碘易升华 |
A. A B. B C. C D. D
【题目】氯化钡是白色的晶体,易溶于水,微溶于盐酸和硝酸,难溶于乙醇和乙醚,易吸湿,需密封保存。工业上制备BaCl2·2H2O有如下两种途径:
途径1:以重晶石(主要成分BaSO4)为原料,流程如下:
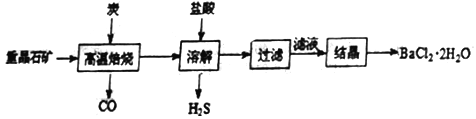
(1)写出“溶解”时反应的化学方程式方程式:________________________。
(2)“高温焙烧”时必须加入过量的炭,同时还要通入空气,其目的是_____________。
(3)结晶得到的晶体,需用乙醇洗涤的理由是_______________________。
途径2:以毒重石(主要成分BaCO3,含CaCO3、MgCO3、Fe2O3、SiO2等杂质)为原料,流程如下:
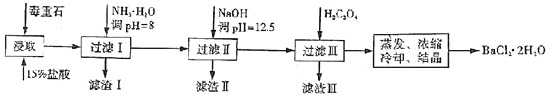
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9,Ksp[Mg(OH)2]=1.8×10-11。
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.7 |
(4)滤渣I的成分为________(填化学式)。
(5)滤渣II中含_________(填化学式)。过滤析出后,滤液中含有的Mg2+浓度为_______。
(6)加入H2C2O4时应避免过量,其原因是为了防止生成______(填化学式)。