题目内容
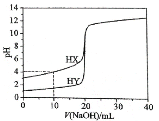
【题目】常温下,用浓度为0.1000mol·L-1的NaOH溶液分别逐滴加入到20.00mL 0.1000mol·L-1的HX、HY溶液中,pH随NaOH溶液体积的变化如图。下列说法正确 ( )
A.V(NaOH)=10.00 mL时,c(X-)>c(Na+)>c(H+)>c(OH-)
B.V(NaOH)=20.00 mL时,两份溶液中,c(X-)>c(Y-)
C.V(NaOH)=20.00 mL时,c(Na+) > c(X-) >c(OH-)>c(H+)
D.pH=7时,两份溶液中,c(X-)=c(Y-)
【答案】AC
【解析】
试题分析:A.V(NaOH)=10.00 mL时,溶液中的溶质为等物质的量的HX和NaX,pH=4,溶液显酸性,说明以HX电离为主,c(X-)>c(Na+)>c(H+)>c(OH-),故A正确;B.0.1000mol·L-1的HX、HY溶液的pH,HX>HY,说明酸性HX<HY ,V(NaOH)=20.00 mL时,溶质均为钠盐,NaX的水解程度大,c(X-)<c(Y-),故B错误;C.V(NaOH)=20.00 mL时,溶质为NaX,NaX的水解,溶液显碱性,c(Na+) > c(X-) >c(OH-)>c(H+),故C正确;D.pH=7时,两份溶液中存在的电荷守恒,分别为c(Na+) +c(H+)= c(X-) +c(OH-)、c(Na+) +c(H+)= c(Y-) +c(OH-),由于酸性HX<HY,pH=7时,消耗的氢氧化钠HX<HY,因此c(X-)<c(Y-),故D错误;故选AC。

练习册系列答案
相关题目