��Ŀ����
Cl2��H2O2�Ǹ��н����������������������������Cl2��������ǿ��H2O2���ܽ�H2O2������Ϊ����֤�ý��ۣ�ѧ�����������ͼ��ʾ��ʵ��װ�ý���ʵ�飨�г�װ����ȥ����Բ����ƿA�еķ�Ӧ����ʽΪ2KMnO4+16HCl��Ũ��=2KCl+2MnCl2+5Cl2��+8H2O����ش���������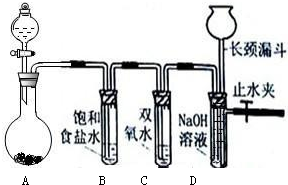
��1���Թ�B�б���ʳ��ˮ������
��2���Թ�C�м���5mL 30%˫��ˮ��������Ӧ�Ļ�ѧ����ʽ
��3���Թ�D�г���10% NaOH��Һ��NaOH��Һ��������
��4����Ũ����ע��Բ����ƿA����װ���еĿ��������ž���ر�ֹˮ�У���Ӧһ��ʱ����Թ�D�е�����Ϊ
��5���е�ͬѧ������ʵ�����Թ�D��������Դ�������ɣ�����Ϊ���ܵ���Դ��
��������1����ʵ������ø�����ع����Ũ����ķ�����ȡ�����������������л����Ȼ��⣬ʹ�ñ���ʳ��ˮ�����ȥ��
��2��Cl2��������ǿ��H2O2���Թ�C���������������ԭ�������Ȼ����������
��3�������ж��������β�������������ͼӦ�����Ȼ��ƺʹ������ƺ�ˮ��
��4�������������ⷴӦ��������������������ˮ����������������ȼ�Խ�����֤������
��5������������ֽ�����������������ˮ��Ӧ��������ʹ����ᣬ������ֽ�����������
��2��Cl2��������ǿ��H2O2���Թ�C���������������ԭ�������Ȼ����������
��3�������ж��������β�������������ͼӦ�����Ȼ��ƺʹ������ƺ�ˮ��
��4�������������ⷴӦ��������������������ˮ����������������ȼ�Խ�����֤������
��5������������ֽ�����������������ˮ��Ӧ��������ʹ����ᣬ������ֽ�����������
����⣺��1����ʵ������ø�����ع����Ũ����ķ�����ȡ�������������������������Ȼ������壬Ҫ��ȥ�Ȼ������壬��ѡ�ij����Լ�ֻ�������Ȼ�������������������ʿ���ʹ�ñ���ʳ��ˮ�����ȥ��
�ʴ�Ϊ����ȥCl2�л��е�HCl��
��2��Cl2��������ǿ��H2O2���Թ�C������������������������������������ԭ���Ȼ��⣬��ӦΪ��Cl2+H2O2=2HCl+O2��
�ʴ�Ϊ��Cl2+H2O2=2HCl+O2��
��3��������һ���о��Ҵ̼�����ζ���ж������壬�����β���������Թ�D�г���10% NaOH��Һ��������NaOH��Һ��ӦCl2+2NaOH=NaCl+NaClO+H2O�����ն����Cl2��
�ʴ�Ϊ�����ն����Cl2��
��4��Cl2+H2O2=2HCl+O2�����ر�ֹˮ�У���Ӧһ��ʱ����Թ�D���������������࣬����ѹǿ���������Թ�D��Һ���½�������©����Һ������������ʹ�����ǵ�ľ����ȼ�����ô˷���֤������
�ʴ�Ϊ���Թ�D��Һ���½�������©����Һ����������������ʹ�����ǵ�ľ����ȼ��֤����������
��5���Թ�D��������Դ����Ϊ��������ķֽ�2H2O2=2H2O+O2����Ҳ����Ϊ����������ˮ��Ӧ��������ʹ����ᣬ������ֽ⣺Cl2+H2O=HCl+HClO��2HClO
2HCl+O2����
�ʴ�Ϊ��2H2O2=2H2O+O2����Cl2+H2O=HCl+HClO��2HClO
2HCl+O2����
�ʴ�Ϊ����ȥCl2�л��е�HCl��
��2��Cl2��������ǿ��H2O2���Թ�C������������������������������������ԭ���Ȼ��⣬��ӦΪ��Cl2+H2O2=2HCl+O2��
�ʴ�Ϊ��Cl2+H2O2=2HCl+O2��
��3��������һ���о��Ҵ̼�����ζ���ж������壬�����β���������Թ�D�г���10% NaOH��Һ��������NaOH��Һ��ӦCl2+2NaOH=NaCl+NaClO+H2O�����ն����Cl2��
�ʴ�Ϊ�����ն����Cl2��
��4��Cl2+H2O2=2HCl+O2�����ر�ֹˮ�У���Ӧһ��ʱ����Թ�D���������������࣬����ѹǿ���������Թ�D��Һ���½�������©����Һ������������ʹ�����ǵ�ľ����ȼ�����ô˷���֤������
�ʴ�Ϊ���Թ�D��Һ���½�������©����Һ����������������ʹ�����ǵ�ľ����ȼ��֤����������
��5���Թ�D��������Դ����Ϊ��������ķֽ�2H2O2=2H2O+O2����Ҳ����Ϊ����������ˮ��Ӧ��������ʹ����ᣬ������ֽ⣺Cl2+H2O=HCl+HClO��2HClO
| ||
�ʴ�Ϊ��2H2O2=2H2O+O2����Cl2+H2O=HCl+HClO��2HClO
| ||
������������Ҫ�����������ͺ�H2O2�����ԵıȽϣ�����������ʵ�����Ʒ���������������ǽ��Ĺؼ�����Ŀ�ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
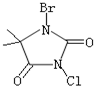 ��2010?����һģ���������й��ס���Ч���Ͷ���ɱ�����������ǽ��չ�����ƣ�
��2010?����һģ���������й��ס���Ч���Ͷ���ɱ�����������ǽ��չ�����ƣ�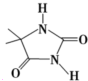
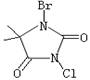 ��3�����庣��C5H6BrClN2O2����һ�ֱȽϰ�ȫ�����������Ƽ��������Ʒ����ṹʽ����ͼ��ʾ��
��3�����庣��C5H6BrClN2O2����һ�ֱȽϰ�ȫ�����������Ƽ��������Ʒ����ṹʽ����ͼ��ʾ��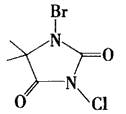
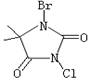 ��3�����庣��C5H6BrClN2O2����һ�ֱȽϰ�ȫ�����������Ƽ��������Ʒ����ṹʽ����ͼ��ʾ��
��3�����庣��C5H6BrClN2O2����һ�ֱȽϰ�ȫ�����������Ƽ��������Ʒ����ṹʽ����ͼ��ʾ��