题目内容
【题目】绿色电源“二甲醚【(CH3)2O】—氧气燃料电池”的工作原理如下图所示,下列说法正确的是( )
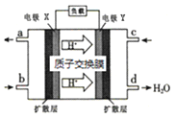
A.氧气应从c处通入,电极Y上发生的反应为:O2+4e-+2H2O=4OH-
B.电池在放电过程中,电极X周围溶液的pH增大
C.当该电池向外电路提供2 mol电子时消耗O2约为11.2L
D.二甲醚应从b处加入,电极X上发生的反应为:(CH3)2O-12e-+3H2O=2CO2+12H+
【答案】D
【解析】
试题分析:A.根据氢离子移动方向知,Y为原电池正极,X为负极,则c处通入的气体是氧气,根据d处生成物知,正极上发生的反应为O2+4e-+4H+=2H2O,电解质溶液为酸性溶液,不可能产生大量的OH-,A错误;B.电池在放电过程中,电极X发生的电极反应为(CH3)2O-12e- +3H2O=2CO2+12H+,X电极周围溶液的pH减小,B错误;C.当该电池向外电路提供2mol电子时消耗O2在标准状况下的体积V(O2)=(2mol÷4)×22.4L/mol=11.2L,由于没有指明气体所处的环境,所以不能计算其体积,C错误;D.二甲醚应从b处加入,X电极上二甲醚失去电子发生氧化反应,所以电极X上发生的反应为((CH3)2O-12e-+3H2O=2CO2+12H+,D正确;答案选D。

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目