题目内容
【题目】利用下图所示装置进行下列实验,能得出相应实验结论的是
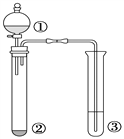
选项 | ① | ② | ③ | 实验结论 |
A | 80%硫酸溶液 | Na2SO3 | 酸性高锰酸钾溶液 | SO2有漂白性 |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性钡盐均可生成白色沉淀 |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:N>C>Si |
A. A B. B C. C D. D
【答案】B
【解析】浓硫酸与Na2SO3反应生成二氧化硫,二氧化硫被酸性高锰酸钾溶液氧化,高锰酸钾溶液褪色,体现了二氧化硫的还原性,不是漂白性,A错误;蔗糖变黑色,说明浓硫酸有脱水性,溴水褪色,说明生成了还原性的SO2,浓硫酸有氧化性,B正确;稀盐酸与Na2SO3反应生成二氧化硫,在酸性环境下,硝酸把二氧化硫氧化为硫酸根离子,从而生成硫酸钡沉淀,但是氯化钡溶液通入二氧化硫气体就不能生成沉淀,因此不能说明SO2与可溶性钡盐均可生成白色沉淀,C错误;浓硝酸与Na2CO3反应生成二氧化碳气体,二氧化碳与硅酸钠溶液反应生成硅酸沉淀,但是硝酸具有挥发性,随着二氧化碳气体一起进入硅酸钠溶液,影响实验,D错误;正确答案B。

 字词句段篇系列答案
字词句段篇系列答案【题目】重金属元素铬的毒性较大,含铬废水需经处理达标后才能排放。已知部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见下表
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9溶解) |
I.某工业废水中主要含有Cr3+,同时还含有少量的Fe2+、Fe3+、Al3+、Ca2+和Mg2+等,且酸性较强。为回收利用,通常采用如下流程处理:

(1)氧化过程中可代替H2O2加入的试剂是________(填序号)。
a.Na2O2 b.HNO3 c.FeCl3 d.KMnO4
(2)加入NaOH溶液调溶液pH=8时,除去的离子是________(填序号);已知钠离子交换树脂的原理:Mn++nNaRMRn+nNa+,此步操作被交换除去的杂质离子__________(填序号)。
a.Fe3+ b.Al3+ c.Ca2+ d.Mg2+
II.酸性条件下,铬元素主要以Cr2O72-形式存在,工业上常用电解法处理含Cr2O72-的废水。该法用Fe、石墨分别作电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3和Fe(OH)3
(3)电解时连接铁棒的一极是电源的_________极。
(4)写出电解时阳极的电极反应式____________________;阳极附近溶液中Cr2O72-转化为Cr3+的离子方程式为______________________________;
(5)常温下,Cr(OH)3的溶度积Ksp=1×10-32,溶液的pH应为________时才能使c(Cr3+)降至1×10-5molL-1