题目内容
100mL 0.2 mol/L NH4Cl溶液,测其pH为a。加蒸馏水稀释至1L后,溶液有关变化错误的是
| A.c(NH4Cl)变为0.02mol/L | B.水的电离程度变大 |
| C.n(Cl-)无变化 | D.pH小于a+1 |
B
试题分析:氯化铵溶于水电离出NH4+、Cl-,其中NH4+水解溶液显酸性。稀释促进水解,据此可以判断。A、稀释过程中溶质不变,因此稀释后c(NH4Cl)=
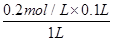 =0.02mol/L,A正确;B、稀释促进水解,但溶液的酸性降低,所以水的电离程度降低,B不正确;C、稀释过程中溶质不变,因此n(Cl-)无变化,C正确;D、稀释促进水解,溶液中氢离子的物质的量增加,所以稀释后溶液中氢离子的浓度大于原来的
=0.02mol/L,A正确;B、稀释促进水解,但溶液的酸性降低,所以水的电离程度降低,B不正确;C、稀释过程中溶质不变,因此n(Cl-)无变化,C正确;D、稀释促进水解,溶液中氢离子的物质的量增加,所以稀释后溶液中氢离子的浓度大于原来的 ,所以pH小于a+1,D正确,答案选B。
,所以pH小于a+1,D正确,答案选B。
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
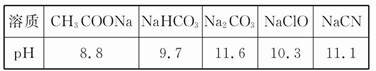
 CH3COOH + OH-水解平衡有影响的是
CH3COOH + OH-水解平衡有影响的是
 CH3COO-+H2O
CH3COO-+H2O