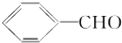
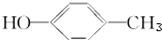
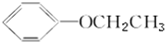题目内容
加入铝能放出H2的溶液中一定可以大量共存的离子组是( )
| A、Al3+、Na+、SO32-、Cl- |
| B、K+、Na+、Cl-、SO42- |
| C、K+、Na+、Cl-、AlO2- |
| D、K+、NH4+、SO42-、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:加入铝能放出H2的溶液中,为非氧化性酸或强碱溶液,根据离子之间不能结合生成沉淀、气体、水,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答:
解:加入铝能放出H2的溶液中,为非氧化性酸或强碱溶液,
A.碱性溶液这不能大量存在Al3+,酸性溶液不能大量存在SO32-,且Al3+、SO32-相互促进水解,不能共存,故A错误;
B.酸或碱溶液中,该组离子之间不反应,可大量共存,故B正确;
C.酸溶液中H+、AlO2-结合生成沉淀,不能大量共存,故C错误;
D.碱性溶液中不能大量存在NH4+,酸溶液中Al、H+、NO3-发生氧化还原反应不生成氢气,故D错误;
故选B.
A.碱性溶液这不能大量存在Al3+,酸性溶液不能大量存在SO32-,且Al3+、SO32-相互促进水解,不能共存,故A错误;
B.酸或碱溶液中,该组离子之间不反应,可大量共存,故B正确;
C.酸溶液中H+、AlO2-结合生成沉淀,不能大量共存,故C错误;
D.碱性溶液中不能大量存在NH4+,酸溶液中Al、H+、NO3-发生氧化还原反应不生成氢气,故D错误;
故选B.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应及氧化还原反应、水解反应的离子共存考查,选项D为解答的难点,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4L H2O所含的原子数目为3NA |
| B、25℃、101.3kPa时,11.2L H2中含有的原子数为NA |
| C、4℃、101.3kPa时,54mL H2O中含有的分子数为3NA |
| D、2L 1mol/L Na2SO4溶液中离子总数为3NA |
下列实验现象描述错误的是( )
| A、H2在Cl2中燃烧发出苍白色火焰 |
| B、将S02通人品红溶液,溶液退色 |
| C、往稀硫酸中滴加酚酞试液,溶液变红色 |
| D、往淀粉溶液中滴加碘水,溶液显蓝色 |
本世纪初,由各国科学家组成的科研小组合成了非常罕见的
Fe原子,你认为关于
Fe的说法中错误的是( )
45 26 |
45 26 |
| A、它位于元素周期表中的第4周期Ⅷ族 | ||||
B、
| ||||
| C、它在氧气中燃烧时失去电子 | ||||
| D、它可表现为+2或+3价 |
常温下,下列各组离子在指定的溶液中可能大量共存的是( )
| A、无色透明溶液中:Al3+、Ca2+、Cl-、HCO3- |
| B、含大量Fe3+的溶液中:K+、I-、SO42-、NO3- |
| C、与Al反应放出H2的溶液中:NH4+、Na+、NO3-、F- |
| D、由水电离出的c(H+)=1.0×10-14mol/L的溶液中:Mg2+、K+、Cl-、SO42- |
W、Z、Y、X四种短周期元素的原子序数依次减少.W、Z位于同周期,原子半径Z大于W;Z、W的最高正价之和等于X的最高正价;W的质子数等于X、Y的质子数之和;W的最高价氧化物对应的水化物与Z、Y的最高价氧化物对应的水化物均能发生反应.下列说法中不正确的是( )
| A、气态氢化物的稳定性:X<Y |
| B、没有X元素也就没有丰富的有机世界 |
| C、非金属性Y>X,金属性W>Z |
| D、在一定条件下,利用X、Z或W单质的还原性,可以冶炼某些金属 |
50mL物质的量浓度为18mol/L的硫酸中加入足量铜片并加热,充分反应,下列有关说法中正确的是( )
| A、有0.9mol的硫酸参加反应 |
| B、有0.45mol的硫酸被还原 |
| C、充分反应后体系无硫酸剩余 |
| D、消耗的铜的质量一定少于28.8g |


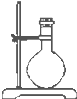


 的物质互为同分异构体的是( )
的物质互为同分异构体的是( )