题目内容
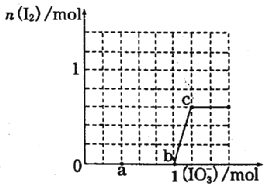
【题目】已知反应:5KI+KIO3+3H2O =3I2+6KOH。其中,还原剂是________(填化学式),被还原的物质是______(填化学式)。若反应中消耗1 mol KIO3,则生成I2____mol。
【答案】 KI KIO3 3
【解析】根据“化合价升高→失电子→还原剂→氧化反应,化合价降低→得电子→氧化剂→还原反应”分析解答。
反应5KI+KIO3+3H2O=3I2+6KOH碘化钾中碘元素化合价从-1价升高到0价,失去电子,被氧化,还原剂是KI,碘酸钾中碘元素化合价从+5价降低到0价,得到电子,作氧化剂,因此被还原的物质是KIO3。根据方程式可知若反应中消耗1 mol KIO3,则生成3 mol I2。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目