题目内容
有一包白色固体粉末,可能含有Na2SO4,CaCO3,KCl,BaCl2,CuSO4中的一种或几种,按以下步骤进行实验:
1.将固体粉末溶于水得到无色溶液和白色沉淀;
2.加以足量的稀盐酸,沉淀部分溶解且有气泡产生。
根据以上实验产生的现象,判断这混合物里,一定含有 物质。一定没有
物质,可能含有的物质 。
写出1的反应方程式
写出2的反应方程式
1.将固体粉末溶于水得到无色溶液和白色沉淀;
2.加以足量的稀盐酸,沉淀部分溶解且有气泡产生。
根据以上实验产生的现象,判断这混合物里,一定含有 物质。一定没有
物质,可能含有的物质 。
写出1的反应方程式
写出2的反应方程式
(10分)一定含有 Na2SO4,CaCO3,BaCl2
一定没有 CuSO4 可能含有 KCl
反应方程式1 Na2SO4 + BaCl2 ="== " BaSO4↓ + 2NaCl
反应方程式2 CaCO3 + 2HCl ="== " CaCl2 + H2O + CO2↑
一定没有 CuSO4 可能含有 KCl
反应方程式1 Na2SO4 + BaCl2 ="== " BaSO4↓ + 2NaCl
反应方程式2 CaCO3 + 2HCl ="== " CaCl2 + H2O + CO2↑
略

练习册系列答案
相关题目
 如下实验:
如下实验: Ca3(
Ca3( PO4)2 + Fe
PO4)2 + Fe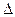 H = -283.0 kJ·mol-2
H = -283.0 kJ·mol-2 + O2(g) ="=" YO2(g)
+ O2(g) ="=" YO2(g)  在溶液中可发生下列反应 NH4+ + OH
在溶液中可发生下列反应 NH4+ + OH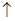 +H2O)
+H2O) 操作中发生先沉淀后溶解现象的是
操作中发生先沉淀后溶解现象的是 中,可不涉及化学变化的是( )
中,可不涉及化学变化的是( )