��Ŀ����
����һ������ˮ��Һ��ֻ���ܺ������������е������֣�K+��NH4+��Cl����Mg2+��Fe3+��CO32����SO42������ÿ��ȡ100ml����ʵ�顣(��֪NH4+��OH ����Һ�пɷ������з�Ӧ NH4+ + OH
����Һ�пɷ������з�Ӧ NH4+ + OH ��NH3
��NH3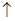 +H2O)
+H2O)
��1����һ�ݼ���AgNO3��Һ�г���������
��2���ڶ��ݼ�����NaOH����ȣ��ռ�������0.896L����״̬�£���
��3�������ݼ�����BaCl2�ø������6.27g����������������ϴ�Ӹ����ʣ2.33g��
�Իش��й����⣺
���ж�K+��Cl���Ƿ���ڣ�K+ Cl�� ����������ţ�
A��һ������ B�����ܴ��� C��һ��������
�ڿ϶����ڵ����ӵ�ԭ��Һ�е����ʵ���Ũ�ȷֱ�Ϊ
��
 ����Һ�пɷ������з�Ӧ NH4+ + OH
����Һ�пɷ������з�Ӧ NH4+ + OH ��NH3
��NH3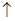 +H2O)
+H2O)��1����һ�ݼ���AgNO3��Һ�г���������
��2���ڶ��ݼ�����NaOH����ȣ��ռ�������0.896L����״̬�£���
��3�������ݼ�����BaCl2�ø������6.27g����������������ϴ�Ӹ����ʣ2.33g��
�Իش��й����⣺
���ж�K+��Cl���Ƿ���ڣ�K+ Cl�� ����������ţ�
A��һ������ B�����ܴ��� C��һ��������
�ڿ϶����ڵ����ӵ�ԭ��Һ�е����ʵ���Ũ�ȷֱ�Ϊ
��
��12�֣�
��1��A B ��2��NH4+ 0.4mol/L SO42- 0.1mol/L CO32- 0.2mol/L K+ >=0.2mol/L
��1��A B ��2��NH4+ 0.4mol/L SO42- 0.1mol/L CO32- 0.2mol/L K+ >=0.2mol/L
��

��ϰ��ϵ�д�
 һ����ʦ�����Ծ�ϵ�д�
һ����ʦ�����Ծ�ϵ�д�
�����Ŀ
 ����ѻ���ɱ�������)��
����ѻ���ɱ�������)��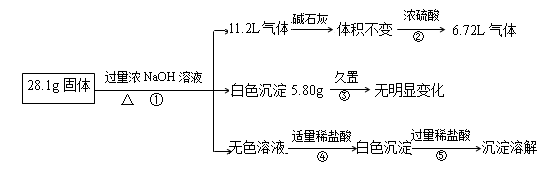
 2Cu+CO2��
2Cu+CO2�� lO
lO