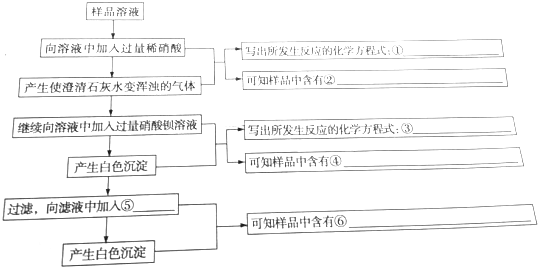
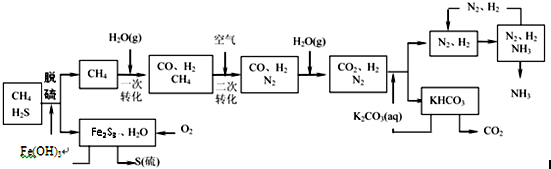
题目内容
6.下列对概念的理解正确的是( )| A. | 二氧化硅可以与碱反应也能与氢氟酸反应,所以二氧化硅属于两性氧化物 | |
| B. | 火碱、苛性钾、纯碱都属于碱 | |
| C. | 离子化合物在熔融状态下都能导电 | |
| D. | 石油分馏、水的汽化、煤的液化都属于物理变化 |
分析 A.二氧化硅既能与氢氟酸反应,又能与烧碱反应,但它是酸性氧化物;
B.纯碱是碳酸钠,属于盐;
C.离子化合物在熔融状态下破坏离子键;
D.物理变化没有新物质生成.
解答 解:A.二氧化硅既能与氢氟酸反应,又能与烧碱反应,但二氧化硅和HF反应生成四氟化硅而不是盐,所以它是酸性氧化物而不是两性氧化物,故A错误;
B.纯碱是碳酸钠,属于盐,不属于碱,故B错误;
C.离子化合物在熔融状态下破坏离子键,能够电离产生自由移动的离子而导电,故C正确;
D.煤液化,是把固体炭通过化学加工过程,使其转化成为液体燃料、化工原料和产品的先进洁净煤技术,有新物质生成,属于化学变化,故D错误;
故选:C.
点评 本题考查了两性氧化物的概念、物理变化与化学变化的区别、酸碱盐的概念、离子化合物的性质,侧重考查学生对基础知识的考查,题目难度不大.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
7.下列离子方程式中正确的是( )
| A. | 将少量SO2气体通入氨水中:SO2+NH3•H2O═NH4++HSO3- | |
| B. | NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O | |
| C. | 向NaOH溶液中滴入少量AlCl3溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | 向稀硫酸加入少量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
8.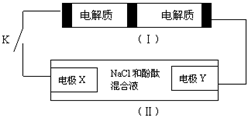 下图装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.装置Ⅰ的离子交换膜只允许Na+通过,已知电池充放电的化学方程式为:
下图装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.装置Ⅰ的离子交换膜只允许Na+通过,已知电池充放电的化学方程式为:
2Na2S2+NaBr3化气 $?_{充电}^{放电}$ Na2S4+3NaBr
当闭合开关K时,X电极附近溶液变红.下列说法正确的是( )
 下图装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.装置Ⅰ的离子交换膜只允许Na+通过,已知电池充放电的化学方程式为:
下图装置Ⅰ是一种可充电电池,装置Ⅱ为电解池.装置Ⅰ的离子交换膜只允许Na+通过,已知电池充放电的化学方程式为:2Na2S2+NaBr3化气 $?_{充电}^{放电}$ Na2S4+3NaBr
当闭合开关K时,X电极附近溶液变红.下列说法正确的是( )
| A. | 闭合开关K时,钠离子从右到左通过离子交换膜 | |
| B. | 闭合开关K时,负极反应式为:3NaBr-2e-═NaBr3+2Na+ | |
| C. | 闭合开关K时,X电极反应式为:2Cl--2e-═Cl2↑ | |
| D. | 闭合开关K时,当有0.1molNa+通过离子交换膜,X电极上析出标准状况下气体1.12L |
11.苯不能使少量酸性高锰酸钾溶液褪色,但苯的同系物能使少量酸性高锰酸钾溶液褪色,下列解释正确的是( )
| A. | 苯的同系物中原子数比苯分子中原子数多 | |
| B. | 苯环受侧链的影响而易被KMnO4氧化 | |
| C. | 侧链受苯环的影响而易被KMnO4氧化 | |
| D. | 苯环和侧链相互影响,同时被氧化 |
18.在反应4NH3+5O2═4NO+6H2O中,下列说法正确的是( )
| A. | NH3在反应中被氧化 | B. | O2在反应中失去电子 | ||
| C. | NH3在反应中得到电子 | D. | 1mol氧化剂在反应中得到4mol电子 |
16.常温下,某柠檬水溶液的pH是4,其中的c(OH-)是( )
| A. | 1×10-4mol/L | B. | 1×10-7mol/L | C. | 1×10-10mol/L | D. | 1×10-11mol/L |