题目内容
(8分)加热19.6克Na2CO3与NaHCO3混合物充分反应后,称量剩余物发现比原来少了3.1 g。试求该19.6克Na2CO3与NaHCO3混合物中二者的物质的量之比。(请写出必要计算过程)
56/53
试题分析:碳酸钠分解。碳酸氢钠受热分解,质量减少。设碳酸氢钠物质的量为xmol。
2NaHCO3
 Na2CO3+H2O+CO2↑ △m
Na2CO3+H2O+CO2↑ △m2mol 18+44=62g
xmol 3.1g
解得x=0.1mol,碳酸氢钠质量为8.4g,碳酸钠质量为11.2g,物质的量为28/265mol,所以碳酸钠和碳酸氢钠物质的量比为56/53。
点评:利用质量差法计算可提高解题速度。

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
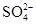 的物质的量浓度是 。
的物质的量浓度是 。