题目内容
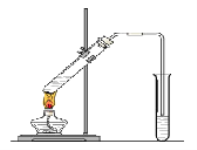
【题目】室温下,将0.10mol·L-1盐酸滴入20.00 mL 0.10mol·L-1氨水中,溶液中pH和pOH随加入盐酸体积变化曲线如图所示。已知:pOH=-lg c(OH-),下列说法正确的是

A. M点所示溶液中c(NH4+)+c(NH3·H2O)=c(Cl-)
B. N点所示溶液中c(NH4+)>c(Cl-)
C. Q点消耗盐酸的体积等于氨水的体积
D. M点和N点所示溶液中水的电离程度相同
【答案】D
【解析】由于Kw=(H+)×c(OH-)=10-14,则溶液的pH+pOH=14,实线为pH曲线,虚线为pOH曲线,作垂直体积坐标轴线与pH曲线、pOH曲线交点为相应溶液中pH、pOH.Q点的pH=pOH,则Q点溶液呈中性. A.M点溶液呈碱性,为NH4Cl、NH3H2O混合溶液,溶液中c(NH4+)+c(NH3H2O)>c(Cl-),A错误; B.N点溶液呈酸性,溶液中(H+)>c(OH-),结合电荷守恒c(NH4+)+c(H+)=c(Cl-)+c(OH-),可知c(NH4+)<c(Cl-),B错误; C.恰好反应得到NH4Cl溶液呈酸性,Q点溶液呈中性,氨水稍过量,C错误;D.M点溶液中氢离子源于水的电离,N点氢氧根离子源于水的电离,而M点氢离子浓度与N点氢氧根离子浓度相等,则M、N点所示溶液中水的电离程度相同,D正确;答案选D。

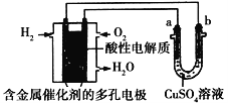
【题目】(1)钠米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂。工业上二氧化钛的制备是:
资料卡片 | ||
物质 | 熔点 | 沸点 |
SiCl4 | -70℃ | 57.6℃ |
TiCl4 | -25℃ | 136.5℃ |
I. 将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应制得混有SiCl4杂质的TiCl4。
II. 将SiCl4分离,得到纯净的TiCl4。
III. 在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O。
IV. TiO2·xH 2O高温分解得到TiO2。
①TiCl4与SiCl4在常温下的状态是________。II中所采取的操作名称是_______。
②III中反应的化学方程式是____________________________________________。
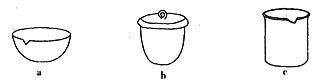
③如IV在实验室完成,应将TiO2·xH2O放在________(填仪器编号)中加热。
(2)根据废水中所含有害物质的不同,工业上有多种废水的处理方法。
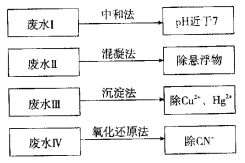
①废水I若采用CO2处理,离子方程式是________________。
②废水Ⅱ常用明矾处理。实践中发现废水中的c(HCO![]() )越大,净水效果越好,这是因为______________。
)越大,净水效果越好,这是因为______________。
③废水III中的汞元素存在如下转化(在空格上填相应的化学式):Hg2++______=CH3Hg++H+,我国规定,Hg2+的排放标准不能超过0.05 mg/L。若某工厂排放的废水1 L中含Hg2+ 3×10-7mo1,是否达到了排放标准__(填“是”或“否”)。
④废水Ⅳ常用C12氧化CN—成CO2和N2,若参加反应的C12 与CN-的物质的量之比为5︰2,则该反应的离子方程式为__________。
【题目】甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇。反应Ⅰ:CO(g)+2H2(g) ![]() CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应Ⅱ:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2
下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K):
温度 | 250 ℃ | 300 ℃ | 350 ℃ |
K | 2.0 | 0.27 | 0.012 |
(1)由表中数据判断ΔH1________(填“>”、“<”或“=”)0;反应CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH3=___________(用ΔH1和ΔH2表示)。
CO(g)+H2O(g) ΔH3=___________(用ΔH1和ΔH2表示)。
(2)若容器容积不变,则下列措施可提高反应Ⅰ中CO转化率的是________(填字母序号)
A.充入CO,使体系总压强增大 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.使用高效催化剂
(3)保持恒温恒容条件对于反应Ⅱ:将10 mol CO2和30mol H2放入1 L的密闭容器中,充分反应后测得CO2的转化率为60%,则该反应的平衡常数为____________________。若维持条件不变向该容器中投入10 mol CO2、30mol H2、10 mol CH3OH(g)和 10mol H2O(g),判断平衡移动的方向是________(填“正向移动”、“逆向移动”或“不移动”)。
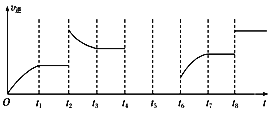
(4)反应Ⅰ的逆反应速率与时间的关系如图所示。由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的条件:t2时_______________________;t8时______________________________。
【题目】碳及其化合物有广泛的用途
(1)甲醇常作燃料,已知在常温常压下甲醇完全燃烧的热化学方程式如下:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH1。则2mol甲醇完全燃烧生成二氧化碳和气态水时反应的ΔH______ΔH1(填“大于”、“等于”或“小于”)
(2)煤的综合利用煤气化是将水蒸气通过红热的碳产生水煤气:C(s)+H2O(g)CO(g)+H2(g) ΔH=+131.3kJ·molˉ1,达到平衡后,下列能提高水煤气生成速率的措施是______。
A.升高温度 B.增加碳的用量 C.缩小体积 D.用CO吸收剂除去CO
(3)一定温度下,将一定量的C(s)和H2O(g)放入某恒容密闭容器中发生上述反应,得到如下数据:
达到平衡所需时间/s | 起始浓度/ mol·Lˉ1 | 平衡浓度/ mol·Lˉ1 |
H2O(g) | H2(g) | |
10 | 2.0 | 0.6 |
计算该反应从开始到平衡时,以CO表示的反应速率为______;H2O(g)的转化率为______。
(4)下列可以说明反应C(s)+H2O(g)CO(g)+H2(g)已经达到平衡状态的是____。
A.单位时间内生成nmolH2的同时,生成nmolCO
B.反应速率: (H2)= (CO)= (H2O)
C.c(H2O):c(CO):c(H2)=1:1:1
D.温度和体积一定时,混合气体的密度不再变化
E.温度和体积一定时,容器内的压强不再变化