题目内容
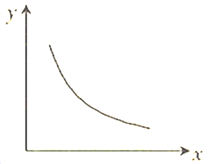
【题目】一定条件下,赤铁矿可用于脱除煤气中的H2S,脱除原理如下:Fe2O3(s)+ 2H2S(g) + H2(g)![]() 2FeS(s)+ 3H2O(g)△H<0。该反应在恒容密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
2FeS(s)+ 3H2O(g)△H<0。该反应在恒容密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
选项 | x | y |
A | 温度 | 平衡常数 |
B | Fe2O3的质量(忽略体积) | H2S的浓度 |
C | 压强 | 混合气体的密度 |
D | n(H2S)/ n(H2) | △H |
A. A B. B C. C D. D
【答案】A
【解析】试题分析: Fe2O3(s)+ 2H2S(g) + H2(g)![]() 2FeS(s)+ 3H2O(g)△H<0,该反应为放热反应,所以温度升高后,其平衡常数减小,A合理;增加氧化铁的质量并不能改变它的浓度,所以平衡不发生移动,H2S的浓度不变,B不合理;反应前后气体的分子数不变,所以增大压强后,平衡不发生移动,但是混合气体的密度增大,C不合理;在一定条件下,△H是定值,不随反应物的投料不同而不同,D不合理。本题选A。
2FeS(s)+ 3H2O(g)△H<0,该反应为放热反应,所以温度升高后,其平衡常数减小,A合理;增加氧化铁的质量并不能改变它的浓度,所以平衡不发生移动,H2S的浓度不变,B不合理;反应前后气体的分子数不变,所以增大压强后,平衡不发生移动,但是混合气体的密度增大,C不合理;在一定条件下,△H是定值,不随反应物的投料不同而不同,D不合理。本题选A。

练习册系列答案
相关题目